レズロック錠 臨床成績
臨床成績
こちらのページでは臨床成績の一部データを掲載しております。
全てのデータをご覧いただく場合は、以下の会員専用サイトをご利用ください。
Meiji Medical Net 医療関係者向け会員サイト
- 一部、用法・用量外の内容を含みますが、承認時評価資料のため紹介します。
- 本剤は、併用薬に応じて、効果不十分な場合に1回200mg1日2回投与に増量できるため、当該投与群のデータを含めて掲載しています。
海外第Ⅱ相試験(KD025-213試験:ROCKstar試験)(海外データ)1)
※「警告・禁忌を含む注意事項等情報」等については電子添文をご参照ください。
1)社内資料:ベルモスジルの海外第Ⅱ相試験(KD025-213試験)(承認時評価資料)
試験概要
†本試験において事前規定された解析時点(治験総括報告書におけるデータカットオフ日)は最終患者登録後6ヵ月経過時点ですが、本情報は承認審査過程で評価された解析時点(データカットオフ日)である最終患者登録後1年経過時点のデータに基づき作成しています。
| 目的 | 過去に2ライン以上の全身治療を受けたことのある慢性移植片対宿主病(慢性GVHD)患者を対象に、レズロックを200mg1日1回又は200mg1日2回投与したときの有効性及び安全性を検討する。 |
|---|---|
| 対象 | ステロイド依存性又は抵抗性の慢性GVHD患者132例 (modified Intention To Treat(mITT)集団※1132例/安全性解析対象集団※1132例) (1日1回投与群:66例、1日2回投与群:66例) レスポンダー集団※299例 (1日1回投与群:48例、1日2回投与群:51例) ※1 レズロックを1回以上投与されたすべての無作為割付患者 ※2 mITT集団においてベースライン(C1D1:サイクル1の1日目)後の総合効果判定で完全奏効(CR)又は部分奏効(PR)を示した患者 |
| 主な選択基準 | 以下のすべての基準に該当する患者を本試験の対象とした。
|
| 主な除外基準 | 以下の基準に一つでも該当する患者は、本試験から除外した。
※3 シロリムス、メトトレキサート、リツキシマブは、本邦において造血幹細胞移植後の慢性移植片対宿主病に対して効能・効果外である。その他の併用可とされた薬剤(ステロイド、CNI、MMF)については、国内承認用法・用量外の症例が一部含まれる。(本試験において使用された各薬剤の国内承認用法・用量については、各製品電子添文をご参照ください。) |
| 試験デザイン | 多施設共同、無作為化、非盲検試験 |
| 方法 | レズロック200mgを1日1回又は1日2回、朝/夕の食事中又は食後5分以内に経口投与した。 本試験は、スクリーニング期(14日)、投与期、追跡調査期(28日)、長期追跡調査期で構成された。 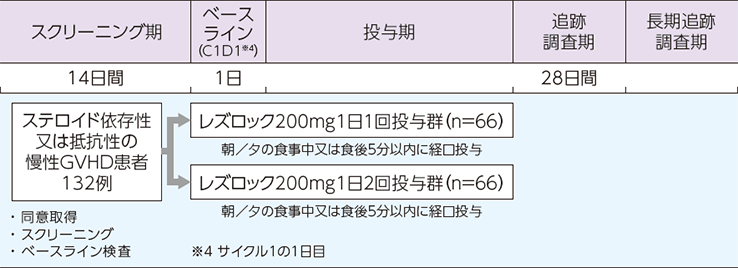
|
| 投与期間 | 新たな全身治療を要する慢性GVHDの進行、基礎疾患である悪性腫瘍の組織学的再発、許容できない安全性上の問題の発現等の投与中止基準に該当するまで投与を継続した。 |
| 有効性評価項目 |
評価項目の定義
評価時点において総合効果がCR又はPRと判定された患者の割合を全奏効率(ORR)、投与期間中のいずれかの評価時点で一度でもCR又はPRと判定された患者の割合をbest ORRと定義した。評価はNIH Consensus Development Project Criteria(2014年)に基づき治験責任医師が行った。
評価項目の定義
臓器別奏効率:各臓器において総合効果がCR又はPR、及び合計(CR+PR)の奏効を示した患者の割合 DOR:総合効果判定で初めてCR又はPRと評価された時点を開始日とし、初めて評価が悪化した時点(CRからPR、又はPRから無効(LR)となった評価時点)までの期間をprimary DORと定義した。また、初めてLRと評価された時点までの期間をsecondary DORと定義した。 TTR:投与開始後から最初にCR又はPRを示した評価時点までの期間 FFS:レズロック初回投与から、慢性GVHDに対する新たな全身治療の開始、基礎疾患である悪性腫瘍の進行・再発、死亡のいずれかが起こるまでの期間 OS:レズロックの初回投与から理由を問わない死亡までの期間 TTNT:レズロックの初回投与から慢性GVHDの新たな全身治療の開始までの期間
|
| 安全性評価項目 | 有害事象、血液学的検査及び生化学検査、バイタルサイン、身体検査、12誘導心電図 |
| 解析計画 | データカットオフ日(最終患者登録後1年経過時)時点†のデータに基づき解析した。
※5 本剤の審査報告書において検討された4項目(感染症、肝機能、血球減少症及び二次性悪性腫瘍)について掲載した。
Gradeの定義
すべての有害事象のGrade は、米国国立がん研究所有害事象共通用語規準(NCI-CTCAE)v5.0の定義に基づき、Grade 1:軽症、Grade 2:中等症、Grade 3:重症、Grade 4:生命を脅かす及びGrade 5:死亡の5段階で評価した。 特に関心のある安全性評価項目の定義
|
allo-HCT:allogeneic hematopoietic cell transplantation、
ROCK2:Rho-associated coiled-coil containing protein kinase 2、
%FEV1:percent predicted forced expiratory volume in one second、
NCI-CTCAE:National Cancer Institute Common Terminology Criteria for Adverse Events、
SMQ:standardised MedDRA queries(MedDRA 標準検索式)、HLGT:high level group terms(高位グループ語)、
HLT:high level terms(高位語)
(1)最良全奏効率(best ORR)(最終患者登録後1年経過時点†)
(主要評価項目):検証的な解析結果
best ORR(最終患者登録後1年経過時点)は、1日1回投与群、1日2回投与群でそれぞれ72.7%(48/66例)、77.3%(51/66例)であった。その95%CIはそれぞれ[60.4, 83.0]、[65.3, 86.7]であり、95%CIの下限値が事前に設定した有効性の判断基準(閾値30%)を上回った。なお、CRは1日1回投与群、1日2回投与群でそれぞれ6.1%(4/66例)、4.5%(3/66例)、PRはそれぞれ66.7%(44/66例)、72.7%(48/66例)であった。
best ORR(最終患者登録後1年経過時点)(mITT集団)
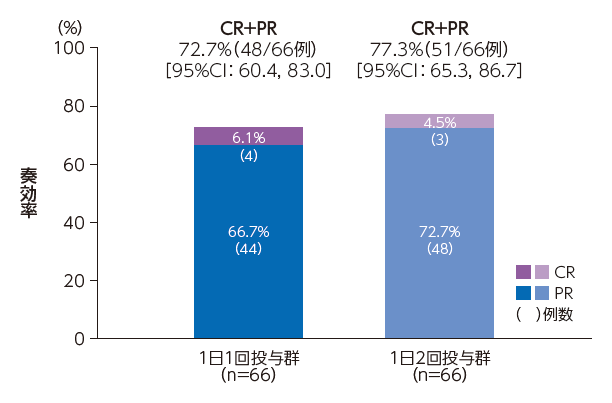
判断基準:best ORRの両側95%CI(Clopper Pearson[正確]法)の下限値が閾値30%を上回った場合
に有効と判断する。
最良総合効果
| 1日1回投与群(n=66) | 1日2回投与群(n=66) | ||
|---|---|---|---|
| best ORR:CR+PR | |||
| 奏効例数、n | 48 | 51 | |
| 奏効率[95%CI] | 72.7%[60.4, 83.0] | 77.3%[65.3, 86.7] | |
評価判定別割合(n)
| 1日1回投与群(n=66) | 1日2回投与群(n=66) | ||
|---|---|---|---|
| CR | 6.1%(4) | 4.5%(3) | |
| PR | 66.7%(44) | 72.7%(48) | |
| LR | |||
| LR-U LR-M LR-P |
21.2%(14) 0 1.5%(1) |
12.1%(8) 4.5%(3) 3.0%(2) |
|
| No response assessment | 4.5%(3) | 3.0%(2) | |
LR:無効、LR-U:無効(不変)、LR-M:無効(改善と悪化の混合)、LR-P:無効(悪化)
†本試験において事前規定された解析時点(治験総括報告書におけるデータカットオフ日)は最終患者登録後6ヵ月経過時点ですが、本情報は承認審査過程で評価された解析時点(データカットオフ日)である最終患者登録後1年経過時点のデータに基づき作成しています。
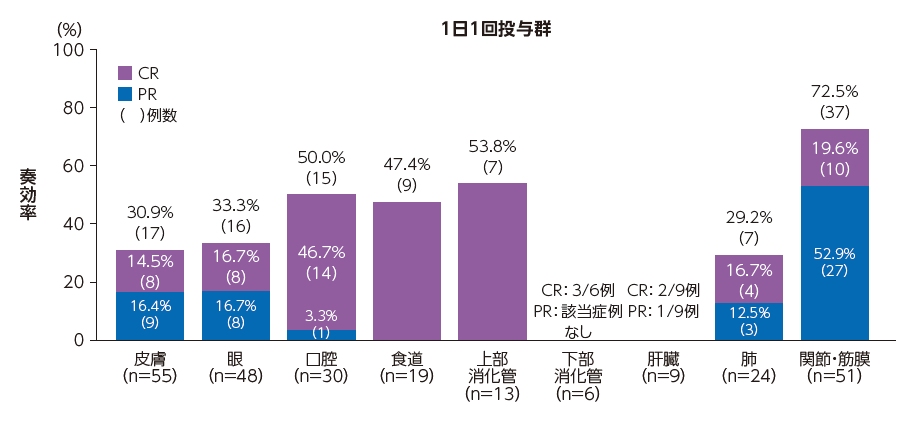
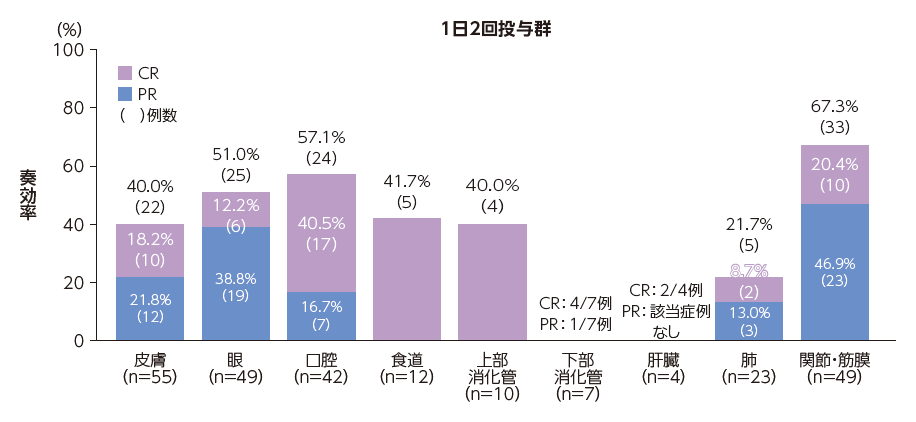
(2)臓器別奏効率(副次評価項目)
評価対象とした罹患臓器のいずれにおいても奏効(PR以上)が認められた。
臓器別奏効率※(mITT集団)
※下部消化管(1日1回投与群:n=6、1日2回投与群:n=7)、肝臓(1日1回投与群:n=9、1日2回投与群:n=4)は10例未満のため、%表記及びグラフ化は行っていない。
(3)安全性
安全性の結果概要(安全性解析対象集団)
1日1回投与群
| 1日1回投与群(n=66) | |||||
| 有害事象 | 副作用 | 概要 | |||
| すべての有害事象及び副作用、 主な副作用 |
65 (98.5) |
49 (74.2) |
主な副作用は疲労17例(25.8%)、悪心9例(13.6%)、下痢、嘔吐、頭痛が各6例(9.1%)であった。 | ||
| 重篤な有害事象 及び副作用 |
27 (40.9) |
5 (7.6) |
重篤な副作用は5例(蜂巣炎、感染性大腸炎、ブドウ球菌性菌血症、肺炎が各1例、下痢、悪心、嘔吐及び多臓器機能不全症候群※1を併発した1例)に認められた。 ※1 死亡症例と同一症例 |
||
| 投与中止に至った有害事象 及び副作用 |
16 (24.2) |
9 (13.6) |
投与中止に至った副作用は9例(悪心3例、疲労、蜂巣炎、好中球減少症、筋痙縮、開口障害※2、食欲減退※3、多臓器機能不全症候群※1、トランスアミナーゼ上昇が各1例)に認められた。 ※1 死亡症例と同一症例 ※2 筋痙縮を発現した症例と同一症例 ※3 悪心を発現した症例と同一症例 |
||
| 死亡に至った有害事象 及び副作用 |
4 (6.1) |
1 (1.5) |
死亡に至った副作用は1例(多臓器機能不全症候群)に認められた。 | ||
n(%)
1日2回投与群
| 1日2回投与群(n=66) | |||||
| 有害事象 | 副作用 | 概要 | |||
| すべての有害事象及び副作用、 主な副作用 |
66 (100.0) |
40 (60.6) |
主な副作用は疲労14例(21.2%)、悪心7例(10.6%)、AST増加6例(9.1%)であった。 | ||
| 重篤な有害事象 及び副作用 |
23 (34.8) |
2 (3.0) |
重篤な副作用は2例(慢性移植片対宿主病※1、微小血管症性溶血性貧血が各1例)に認められた。 ※1 死亡症例と同一症例 |
||
| 投与中止に至った有害事象 及び副作用 |
12 (18.2) |
7 (10.6) |
投与中止に至った副作用は7例(AST増加、頭痛、潰瘍性角膜炎、微小血管症性溶血性貧血、疲労、激越が各1例、ALT増加及びAST増加を併発した1例)に認められた。 | ||
| 死亡に至った有害事象 及び副作用 |
4 (6.1) |
1 (1.5) |
死亡に至った副作用は1例(慢性移植片対宿主病)に認められた。 | ||
n(%)
AST:アスパラギン酸アミノトランスフェラーゼ、ALT:アラニンアミノトランスフェラーゼ
主な有害事象及び副作用の内訳(いずれかの群で有害事象発現率10%以上)
1日1回投与群及び1日2回投与群
| 1日1回投与群(n=66) | 1日2回投与群(n=66) | |||||||
| 有害事象 | 副作用 | 有害事象 | 副作用 | |||||
| 器官別大分類(SOC) 基本語(PT) |
全Grade | Grade 3以上 | 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | 全Grade | Grade 3以上 |
| すべての有害事象および副作用 | 65 (98.5) |
37 (56.1) |
49 (74.2) |
13 (19.7) |
66 (100.0) |
34 (51.5) |
40 (60.6) |
10 (15.2) |
| 一般・全身障害および投与部位の状態 | 45 (68.2) |
6 (9.1) |
20 (30.3) |
2 (3.0) |
36 (54.5) |
6 (9.1) |
19 (28.8) |
3 (4.5) |
| 疲労 | 30 (45.5) |
2 (3.0) |
17 (25.8) |
1 (1.5) |
20 (30.3) |
3 (4.5) |
14 (21.2) |
3 (4.5) |
| 末梢性浮腫 | 17 (25.8) |
1 (1.5) |
2 (3.0) |
- | 13 (19.7) |
1 (1.5) |
4 (6.1) |
- |
| 発熱 | 14 (21.2) |
1 (1.5) |
2 (3.0) |
- | 6 (9.1) |
- | 1 (1.5) |
- |
| 胃腸障害 | 50 (75.8) |
12 (18.2) |
19 (28.8) |
6 (9.1) |
47 (71.2) |
6 (9.1) |
13 (19.7) |
1 (1.5) |
| 悪心 | 23 (34.8) |
2 (3.0) |
9 (13.6) |
1 (1.5) |
18 (27.3) |
2 (3.0) |
7 (10.6) |
1 (1.5) |
| 下痢 | 23 (34.8) |
3 (4.5) |
6 (9.1) |
2 (3.0) |
21 (31.8) |
- | 5 (7.6) |
- |
| 嘔吐 | 18 (27.3) |
2 (3.0) |
6 (9.1) |
1 (1.5) |
10 (15.2) |
1 (1.5) |
1 (1.5) |
- |
| 便秘 | 7 (10.6) |
1 (1.5) |
4 (6.1) |
1 (1.5) |
5 (7.6) |
- | 1 (1.5) |
- |
| 腹痛 | 11 (16.7) |
1 (1.5) |
2 (3.0) |
- | 7 (10.6) |
1 (1.5) |
1 (1.5) |
- |
| 腹部膨満 | 7 (10.6) |
- | 2 (3.0) |
- | - | - | - | - |
| 口内乾燥 | 8 (12.1) |
1 (1.5) |
1 (1.5) |
1 (1.5) |
5 (7.6) |
- | 1 (1.5) |
- |
| 嚥下障害 | 13 (19.7) |
- | - | - | 1 (1.5) |
- | - | - |
| 呼吸器、胸郭 および縦隔障害 |
42 (63.6) |
9 (13.6) |
7 (10.6) |
1 (1.5) |
41 (62.1) |
4 (6.1) |
5 (7.6) |
- |
| 呼吸困難 | 21 (31.8) |
2 (3.0) |
4 (6.1) |
- | 12 (18.2) |
1 (1.5) |
1 (1.5) |
- |
| 咳嗽 | 20 (30.3) |
- | 2 (3.0) |
- | 17 (25.8) |
- | 3 (4.5) |
- |
| 湿性咳嗽 | 8 (12.1) |
- | - | - | 7 (10.6) |
- | 1 (1.5) |
- |
| 鼻閉 | 7 (10.6) |
- | - | - | 8 (12.1) |
- | - | - |
| 感染症および 寄生虫症 |
41 (62.1) |
13 (19.7) |
10 (15.2) |
3 (4.5) |
39 (59.1) |
10 (15.2) |
5 (7.6) |
- |
| 上気道感染 | 17 (25.8) |
- | 2 (3.0) |
- | 18 (27.3) |
1 (1.5) |
2 (3.0) |
- |
| 肺炎 | 7 (10.6) |
6 (9.1) |
1 (1.5) |
1 (1.5) |
7 (10.6) |
4 (6.1) |
1 (1.5) |
- |
| 筋骨格系および結合組織障害 | 37 (56.1) |
4 (6.1) |
10 (15.2) |
- | 38 (57.6) |
1 (1.5) |
6 (9.1) |
- |
| 筋痙縮 | 13 (19.7) |
- | 2 (3.0) |
- | 13 (19.7) |
- | 3 (4.5) |
- |
| 関節痛 | 12 (18.2) |
2 (3.0) |
2 (3.0) |
- | 8 (12.1) |
- | 4 (6.1) |
- |
| 四肢痛 | 8 (12.1) |
1 (1.5) |
- | - | 10 (15.2) |
- | 1 (1.5) |
- |
| 背部痛 | 7 (10.6) |
2 (3.0) |
2 (3.0) |
- | 7 (10.6) |
1 (1.5) |
1 (1.5) |
- |
| 神経系障害 | 24 (36.4) |
2 (3.0) |
12 (18.2) |
- | 31 (47.0) |
4 (6.1) |
14 (21.2) |
2 (3.0) |
| 頭痛 | 13 (19.7) |
- | 6 (9.1) |
- | 18 (27.3) |
2 (3.0) |
5 (7.6) |
1 (1.5) |
| 浮動性めまい | 5 (7.6) |
- | 1 (1.5) |
- | 8 (12.1) |
- | 2 (3.0) |
- |
| 代謝および 栄養障害 |
33 (50.0) |
9 (13.6) |
13 (19.7) |
1 (1.5) |
27 (40.9) |
6 (9.1) |
8 (12.1) |
- |
| 食欲減退 | 12 (18.2) |
1 (1.5) |
5 (7.6) |
1 (1.5) |
5 (7.6) |
- | 2 (3.0) |
- |
| 高血糖 | 10 (15.2) |
3 (4.5) |
4 (6.1) |
- | 12 (18.2) |
3 (4.5) |
2 (3.0) |
- |
| 血管障害 | 20 (30.3) |
7 (10.6) |
3 (4.5) |
3 (4.5) |
24 (36.4) |
6 (9.1) |
6 (9.1) |
2 (3.0) |
| 高血圧 | 12 (18.2) |
4 (6.1) |
1 (1.5) |
1 (1.5) |
11 (16.7) |
4 (6.1) |
4 (6.1) |
2 (3.0) |
| 皮膚および 皮下組織障害 |
28 (42.4) |
1 (1.5) |
2 (3.0) |
- | 26 (39.4) |
- | 5 (7.6) |
- |
| そう痒症 | 8 (12.1) |
- | 1 (1.5) |
- | 9 (13.6) |
- | 4 (6.1) |
- |
| 傷害、中毒および処置合併症 | 25 (37.9) |
3 (4.5) |
1 (1.5) |
- | 19 (28.8) |
- | - | - |
| 挫傷 | 8 (12.1) |
- | 1 (1.5) |
- | 3 (4.5) |
- | - | - |
| 転倒 | 7 (10.6) |
2 (3.0) |
- | - | 8 (12.1) |
- | - | - |
| 血液および リンパ系障害 |
8 (12.1) |
3 (4.5) |
3 (4.5) |
1 (1.5) |
11 (16.7) |
4 (6.1) |
3 (4.5) |
2 (3.0) |
| 貧血 | 5 (7.6) |
2 (3.0) |
2 (3.0) |
- | 8 (12.1) |
2 (3.0) |
1 (1.5) |
- |
| 臨床検査 | 29 (43.9) |
6 (9.1) |
17 (25.8) |
1 (1.5) |
32 (48.5) |
2 (3.0) |
15 (22.7) |
1 (1.5) |
| γ-グルタミルトランスフェラーゼ増加 | 6 (9.1) |
2 (3.0) |
3 (4.5) |
1 (1.5) |
10 (15.2) |
1 (1.5) |
3 (4.5) |
- |
| AST増加 | 5 (7.6) |
- | 4 (6.1) |
- | 8 (12.1) |
1 (1.5) |
6 (9.1) |
1 (1.5) |
| 血中クレアチニン増加 | 5 (7.6) |
- | 2 (3.0) |
- | 7 (10.6) |
- | 2 (3.0) |
- |
| ALT増加 | 4 (6.1) |
- | 3 (4.5) |
- | 7 (10.6) |
- | 5 (7.6) |
- |
MedDRA/J version 20.0
n(%)
Grade:NCI-CTCAE v5.0
AST:アスパラギン酸アミノトランスフェラーゼ、ALT:アラニンアミノトランスフェラーゼ
器官別大分類(SOC)では、基本語(PT)を複数事象発現した症例は1例としてカウントした。
同一事象が同一患者に複数回発現した場合は、Gradeが最も高い事象を1回のみカウントした。
特に関心のある安全性評価項目
1日1回投与群
| 1日1回投与群(n=66) | ||
| 有害事象 | 概要 | |
| 感染症に 関連する有害事象 |
41 (62.1) |
|
| 肝機能に 関連する有害事象 |
12 (18.2) |
|
| 血球減少症に 関連する有害事象 |
7 (10.6) |
|
| 二次性悪性腫瘍に 関連する有害事象 |
6 (9.1) |
|
n(%)
※ 治験薬との関連性ありと判定された有害事象は認められなかった。
1日2回投与群
| 1日2回投与群(n=66) | ||
| 有害事象 | 概要 | |
| 感染症に 関連する有害事象 |
39 (59.1) |
|
| 肝機能に 関連する有害事象 |
16 (24.2) |
|
| 血球減少症に 関連する有害事象 |
14 (21.2) |
|
| 二次性悪性腫瘍に 関連する有害事象 |
3 (4.5) |
|
n(%)
※ 治験薬との関連性ありと判定された有害事象は認められなかった。
AST:アスパラギン酸アミノトランスフェラーゼ、ALT:アラニンアミノトランスフェラーゼ
- 6. 用法・用量
通常、成人及び12歳以上の小児にはベルモスジルとして200mgを1日1回食後に経口投与する。併用薬に応じて、効果不十分な場合に1回200mg1日2回投与に増量できる。 - 7. 用法・用量に関連する注意
- 7.1 食後投与に比べて空腹時投与で本剤のCmax及びAUCが低下するため、本剤は食後に服用すること。[16.2.1 参照]
- 7.2 プロトンポンプ阻害剤又は強いCYP3A4誘導剤との併用により、本剤の血中濃度が低下する可能性があるため、これらの薬剤を併用する場合は患者の状態に注意し、本剤の効果が不十分な場合には、本剤を1回200mg1日2回投与に増量することを考慮すること。[10.2、16.7.1-16.7.3 参照]
- 8. 重要な基本的注意(一部抜粋)
- 8.2 肝機能障害があらわれることがあるので、本剤投与中は定期的に肝機能検査を実施すること。
- 9. 特定の背景を有する患者に関する注意(一部抜粋)
- 9.3 肝機能障害患者
- 9.3.1 重度(Child-Pugh分類C)の肝機能障害患者
可能な限り投与を避けること。やむを得ず投与する場合には、患者の状態をより慎重に観察し、有害事象の発現に十分注意すること。本剤の血中濃度が上昇し、副作用が強くあらわれるおそれがある。[16.6.1 参照]
国内第Ⅲ相試験(ME3208-2試験)2)
2)社内資料:ベルモスジルの国内第Ⅲ相試験(ME3208-2試験)(承認時評価資料)
試験概要
本情報は、データカットオフ日(最終患者登録後24週経過時)時点のデータに基づき作成した。
| 目的 | ステロイド依存性又は抵抗性の慢性移植片対宿主病(慢性GVHD)患者を対象に、レズロックの有効性及び安全性を検討する。 |
|---|---|
| 対象 | ステロイド依存性又は抵抗性の慢性GVHD患者21例 (modified Intention To Treat(mITT)集団※121例/PPS(Per Protocol Set)集団※221例/ 安全性解析対象集団※321例) レスポンダー集団※418例 ※1 治療期開始以降に最低1回の投与が確認された患者 ※2 治験実施計画書に定めた治験スケジュールを遵守し、重大な治験実施計画書違反がない患者 ※3 レズロックが1回以上投与されたステロイド依存性又は抵抗性の慢性GVHD患者 ※4 mITT集団においてベースライン(Visit2:第2来院日)後の総合効果判定で完全奏効(CR)又は部分奏効(PR)を示した患者 |
| 主な選択基準 | 以下のすべての基準に該当する患者を本試験の対象とした。
|
| 主な除外基準 | 以下の基準に一つでも該当する患者は、本試験から除外した。
|
| 試験デザイン | 多施設共同、非盲検、単群試験 |
| 方法 | レズロック200mgを1日1回、食後に経口投与した。 本試験は、観察期(28日以内)、治療期、後観察期(28日)、追跡調査期で構成された。 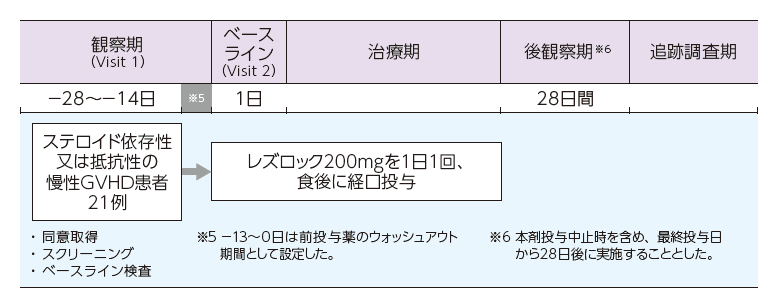 |
| 投与期間 | 疾患進行又は許容できない有害事象の発現等の投与中止基準に該当するまで投与を継続した。 |
| 有効性評価項目 |
評価項目の定義
評価時点において総合効果がCR又はPRと判定された患者の割合を全奏効率(ORR)、投与期間中のいずれかの評価時点で一度でもCR又はPRと判定された患者の割合をbest ORRと定義した。評価はNIH Consensus Development Project Criteria(2014年)に基づき治験責任医師が行った。
評価項目の定義
臓器別奏効率:各臓器において総合効果がCR又はPR、及び合計(CR+PR)の奏効を示した患者の割合 DOR:総合効果判定で初めてCR又はPRと評価された時点を開始日とし、初めて評価が悪化した時点(CRからPR、又はPRから無効(LR)となった評価時点)、慢性GVHDに対する新たな全身治療の開始又は死亡のいずれか早い時点までの期間をprimary DORと定義した。また、初めてLRと評価された時点、慢性GVHDに対する新たな全身治療の開始又は死亡のいずれか早い時点までの期間をsecondary DORと定義した。 TTR:投与開始後から最初にCR又はPRを示した評価時点までの期間 FFS:レズロック初回投与から、慢性GVHDに対する新たな全身治療の開始、基礎疾患である悪性腫瘍の進行・再発、死亡のいずれかが起こるまでの期間と定義した。なお、慢性GVHDの新たな全身治療の開始は、ステロイド増量がプレドニゾロン換算で1mg/日未満の場合及びその他の免疫抑制剤の種類を変更した場合は含まないこととした。 OS: レズロックの初回投与から理由を問わない死亡までの期間
評価項目の定義
TTNT:レズロックの初回投与から慢性GVHDの新たな全身治療の開始までの期間
|
| 安全性評価項目 | 有害事象、血液学的検査及び生化学検査、バイタルサイン、体重、12誘導心電図 |
| 解析計画 | データカットオフ日(最終患者登録後24週経過時)時点のデータに基づき解析した。
※7 本剤の審査報告書において検討された4項目(感染症、肝機能、血球減少症及び二次性悪性腫瘍)について掲載した。 Gradeの定義
すべての有害事象のGrade は、有害事象共通用語規準(CTCAE)v5.0 日本語訳日本腫瘍研究グループ(JCOG)版(CTCAE v5.0-JCOG)の定義に基づき、Grade 1:軽症、Grade 2:中等症、Grade 3:重症、Grade 4:生命を脅かす及びGrade 5:死亡の5段階で評価した。 特に関心のある安全性評価項目の定義
|
allo-HCT:allogeneic hematopoietic cell transplantation、
%FEV1:percent predicted forced expiratory volume in one second、
CTCAE:Common Terminology Criteria for Adverse Events、
JCOG:Japan Clinical Oncology Group、
SMQ:standardised MedDRA queries(MedDRA 標準検索式)、
HLGT:high level group terms(高位グループ語)、
HLT:high level terms(高位語)
(1)最良全奏効率(best ORR)(最終患者登録後24週経過時点)
(主要評価項目):検証的な解析結果
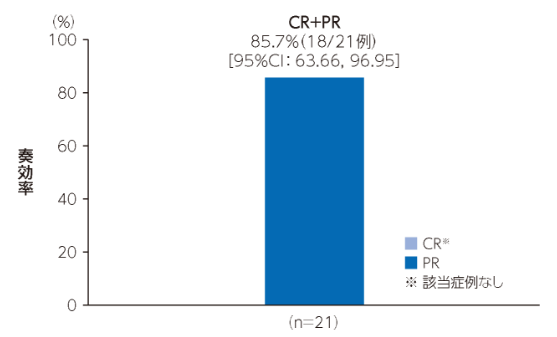
best ORR(最終患者登録後24週経過時点)は85.7%(18/21例)であった。その95%CIは[63.66,96.95]であり、95%CIの下限値が事前に設定した有効性の判断基準(閾値25%)を上回った。なお、奏効が得られた患者の最良全奏効は、すべてPRであった。
best ORR(最終患者登録後24週経過時点)(mITT集団、PPS集団)
判断基準:best ORRの両側95%CI(Clopper Pearson[正確]法)の下限値が閾値25%を上回
った場合に有効と判断する。
最良総合効果
| n=21 | ||
|---|---|---|
| best ORR:CR+PR | ||
| 奏効例数、n | 18 | |
| 奏効率[95%CI] | 85.7%[63.66, 96.95] | |
評価判定別割合(n)
| n=21 | ||
|---|---|---|
| CR | 0 | |
| PR | 85.7%(18) | |
| LR | LR-U LR-M LR-P |
14.3%(3) 0 0 |
| No response assessment | 0 | |
LR:無効、LR-U:無効(不変)、LR-M:無効(改善と悪化の混合)、LR-P:無効(悪化)
(2)臓器別奏効率(副次評価項目)
臓器別奏効率は、皮膚54.5%(6/11例)、眼20.0%(3/15例)、口腔66.7%(12/18例)、食道が2例中1例、上部消化管が1例中1例、関節・筋膜が5例中4例であった。下部消化管及び肺では奏効が認められなかった。なお、本試験に登録された患者において肝臓に病変を有する患者は含まれなかった。
臓器別奏効率(mITT集団、PPS集団)
最良総合効果
| n | CR | PR | 奏効 (CR+PR) |
||
| 臓器別 奏効率 |
皮膚 | 11 | 2(18.2) | 4(36.4) | 6(54.5) |
| 眼 | 15 | 1(6.7) | 2(13.3) | 3(20.0) | |
| 口腔 | 18 | 6(33.3) | 6(33.3) | 12(66.7) | |
| 食道 | 2 | 1 | 0 | 1 | |
| 上部消化管 | 1 | 1 | 0 | 1 | |
| 下部消化管 | 1 | 0 | 0 | 0 | |
| 肝臓 | 0※ | - | - | - | |
| 肺 | 6 | 0 | 0 | 0 | |
| 関節・筋膜 | 5 | 1 | 3 | 4 | |
n(%)
※ 本試験に登録された患者において肝臓に病変を有する患者は含まれなかった。
(3)安全性(安全性解析対象集団)
安全性の結果概要
| 安全性解析対象集団(n=21) | |||||
| 有害事象 | 副作用 | 概要 | |||
| すべての有害事象及び副作用、 主な副作用 |
18 (85.7) |
8 (38.1) |
主な副作用は帯状疱疹、筋痙縮が各2例(9.5%)であった。 | ||
| 重篤な有害事象及び副作用 | 6 (28.6) |
1 (4.8) |
重篤な副作用は1例(肺炎)に認められた。 | ||
| 投与中止に至った有害事象 及び副作用 |
1 (4.8) |
- | 投与中止に至った有害事象は1例(縦隔の悪性新生物、再発急性骨髄性白血病※)に認められたが、治験薬との関連性なしと判定された。 ※ 同一症例 |
||
| 死亡に至った有害事象 及び副作用 |
1 (4.8) |
- | 死亡に至った有害事象は1例(再発急性骨髄性白血病)に認められたが、治験薬との関連性なしと判定された。 | ||
n(%)
有害事象及び副作用の内訳
| 安全性解析対象集団(n=21) | ||||
| 有害事象 | 副作用 | |||
| 器官別大分類(SOC) 基本語(PT) |
全Grade | Grade 3以上 | 全Grade | Grade 3以上 |
| すべての有害事象および副作用 | 18(85.7) | 6(28.6) | 8(38.1) | 1(4.8) |
| 筋骨格系および結合組織障害 | 8(38.1) | - | 2(9.5) | - |
| 背部痛 | 2(9.5) | - | - | - |
| 筋痙縮 | 2(9.5) | - | 2(9.5) | - |
| 筋肉痛 | 2(9.5) | - | - | - |
| 関節痛 | 1(4.8) | - | - | - |
| 変形性脊椎症 | 1(4.8) | - | - | - |
| 感染症および寄生虫症 | 9(42.9) | 5(23.8) | 3(14.3) | 1(4.8) |
| 帯状疱疹 | 3(14.3) | - | 2(9.5) | - |
| COVID-19 | 3(14.3) | 2(9.5) | - | - |
| 気管支炎 | 1(4.8) | 1(4.8) | - | - |
| 気管支肺アスペルギルス症 | 1(4.8) | 1(4.8) | - | - |
| 咽頭炎 | 1(4.8) | - | - | - |
| 肺炎 | 1(4.8) | 1(4.8) | 1(4.8) | 1(4.8) |
| 誤嚥性肺炎 | 1(4.8) | 1(4.8) | - | - |
| 敗血症 | 1(4.8) | 1(4.8) | - | - |
| 胃腸障害 | 5(23.8) | 2(9.5) | 1(4.8) | - |
| 下痢 | 4(19.0) | - | 1(4.8) | - |
| 上腹部痛 | 1(4.8) | - | - | - |
| イレウス | 1(4.8) | 1(4.8) | - | - |
| 嘔吐 | 1(4.8) | - | - | - |
| 大腸ポリープ | 1(4.8) | - | - | - |
| 胃腸ポリープ | 1(4.8) | 1(4.8) | - | - |
| 眼障害 | 4(19.0) | 1(4.8) | 1(4.8) | - |
| 白内障 | 3(14.3) | 1(4.8) | - | - |
| 結膜出血 | 1(4.8) | - | 1(4.8) | - |
| 網膜出血 | 1(4.8) | - | 1(4.8) | - |
| 網脈絡膜症 | 1(4.8) | - | - | - |
| 代謝および栄養障害 | 4(19.0) | - | - | - |
| 低カリウム血症 | 2(9.5) | - | - | - |
| 耐糖能障害 | 1(4.8) | - | - | - |
| 高トリグリセリド血症 | 1(4.8) | - | - | - |
| 脂質異常症 | 1(4.8) | - | - | - |
| 皮膚および皮下組織障害 | 4(19.0) | - | 1(4.8) | - |
| 蕁麻疹 | 2(9.5) | - | 1(4.8) | - |
| 湿疹 | 1(4.8) | - | - | - |
| 発疹 | 1(4.8) | - | - | - |
| 一般・全身障害および投与部位の状態 | 3(14.3) | - | 1(4.8) | - |
| 浮腫 | 2(9.5) | - | 1(4.8) | - |
| 発熱 | 1(4.8) | - | - | - |
| 傷害、中毒および処置合併症 | 3(14.3) | - | - | - |
| 凍瘡 | 1(4.8) | - | - | - |
| 靱帯捻挫 | 1(4.8) | - | - | - |
| 皮膚裂傷 | 1(4.8) | - | - | - |
| 神経系障害 | 2(9.5) | - | 1(4.8) | - |
| 頭痛 | 1(4.8) | - | 1(4.8) | - |
| 神経系障害 | 1(4.8) | - | - | - |
| 精神障害 | 2(9.5) | - | - | - |
| うつ病 | 1(4.8) | - | - | - |
| 不眠症 | 1(4.8) | - | - | - |
| 腎および尿路障害 | 2(9.5) | - | - | - |
| 腎機能障害 | 1(4.8) | - | - | - |
| 尿管結石症 | 1(4.8) | - | - | - |
| 呼吸器、胸郭および縦隔障害 | 2(9.5) | - | - | - |
| 鼻出血 | 1(4.8) | - | - | - |
| 気管狭窄 | 1(4.8) | - | - | - |
| 血管障害 | 2(9.5) | - | - | - |
| 静脈炎 | 1(4.8) | - | - | - |
| 血管炎 | 1(4.8) | - | - | - |
| 血液およびリンパ系障害 | 1(4.8) | - | - | - |
| 低グロブリン血症 | 1(4.8) | - | - | - |
| 心臓障害 | 1(4.8) | 1(4.8) | - | - |
| 心不全 | 1(4.8) | 1(4.8) | - | - |
| 良性、悪性および詳細不明の新生物 (嚢胞およびポリープを含む) |
1(4.8) | 1(4.8) | - | - |
| 再発急性骨髄性白血病 | 1(4.8) | 1(4.8) | - | - |
| 縦隔の悪性新生物 | 1(4.8) | 1(4.8) | - | - |
| 臨床検査 | 5(23.8) | - | 3(14.3) | - |
| アミラーゼ増加 | 1(4.8) | - | 1(4.8) | - |
| 血中コレステロール増加 | 1(4.8) | - | - | - |
| 血中クレアチニン増加 | 1(4.8) | - | 1(4.8) | - |
| 心電図ST部分上昇 | 1(4.8) | - | 1(4.8) | - |
| プロトロンビン時間短縮 | 1(4.8) | - | - | - |
MedDRA/J version 24.1
n(%)
Grade:CTCAE v5.0-JCOG
器官別大分類(SOC)では、基本語(PT)を複数事象発現した症例は1例としてカウントした。
同一事象が同一患者に複数回発現した場合は、Gradeが最も高い事象を1回のみカウントした。
特に関心のある安全性評価項目
| 安全性解析対象集団(n=21) | ||
| 有害事象 | 概要 | |
| 感染症に 関連する有害事象 |
9 (42.9) |
|
| 肝機能に 関連する有害事象 |
ー |
|
| 血球減少症に 関連する有害事象 |
ー |
|
| 二次性悪性腫瘍に 関連する有害事象 |
1 (4.8) |
|
n(%)
※ 治験薬との関連性ありと判定された有害事象は認められなかった。
- 4. 効能・効果
造血幹細胞移植後の慢性移植片対宿主病(ステロイド剤の投与で効果不十分な場合) - 6. 用法・用量
通常、成人及び12歳以上の小児にはベルモスジルとして200mgを1日1回食後に経口投与する。併用薬に応じて、効果不十分な場合に1回200mg1日2回投与に増量できる。 - 7. 用法・用量に関連する注意
- 7.1 食後投与に比べて空腹時投与で本剤のCmax及びAUCが低下するため、本剤は食後に服用すること。[16.2.1 参照]
- 7.2 プロトンポンプ阻害剤又は強いCYP3A4誘導剤との併用により、本剤の血中濃度が低下する可能性があるため、これらの薬剤を併用する場合は患者の状態に注意し、本剤の効果が不十分な場合には、本剤を1回200mg1日2回投与に増量することを考慮すること。[10.2、16.7.1-16.7.3 参照]
- 8. 重要な基本的注意(一部抜粋)
- 8.2 肝機能障害があらわれることがあるので、本剤投与中は定期的に肝機能検査を実施すること。
- 9. 特定の背景を有する患者に関する注意(一部抜粋)
- 9.3 肝機能障害患者
- 9.3.1 重度(Child-Pugh分類C)の肝機能障害患者
可能な限り投与を避けること。やむを得ず投与する場合には、患者の状態をより慎重に観察し、有害事象の発現に十分注意すること。本剤の血中濃度が上昇し、副作用が強くあらわれるおそれがある。[16.6.1 参照]
閲覧履歴
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。
あなたは医療関係者ですか?
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。


 くすりに関する
くすりに関する