ハイヤスタ錠 薬効薬理
薬効薬理
1.作用機序22),23)
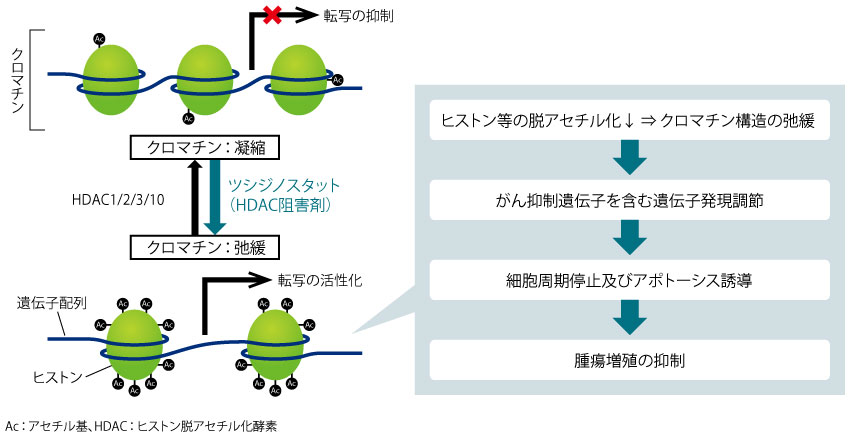
ツシジノスタットは、ヒストン脱アセチル化酵素(HDAC)であるHDAC1、HDAC2及びHDAC3(クラスⅠ)、並びにHDAC10(クラスⅡb)の酵素活性を阻害する22)。HDAC活性阻害によりヒストン等の脱アセチル化が阻害され、細胞周期停止及びアポトーシス誘導が生じることにより、腫瘍増殖が抑制されると推測されている。しかし、詳細な作用機序は解明されていない。
ツシジノスタットは、in vitroにおいて、ATL由来初代細胞に対して、増殖抑制作用を示した23)。
■ツシジノスタットの作用機序
-
- 22)Ning Z-Q, et al.: Cancer Chemother Pharmacol. 2012; 69(4): 901-9. Newman MJはHUYA Bioscience International, LLCに所属している。
- 23)Hasegawa H, et al.: Cancer Sci. 2016; 107(8): 1124-33.
- Hasegawa HはHUYA Bioscience International, LLCから研究費を受領している。
- Bissonnette RPはHUYA Bioscience International, LLCの社員である。
- Gillings MはHUYA Bioscience International, LLCで役職に就いている。
2. 臨床薬理試験
-
(1)ヒストンH3(H-3)に対する作用(固形がん/リンパ腫、海外データ)24)
固形がん又はリンパ腫を有する中国人患者にツシジノスタット25mg、32.5mg又は50mgを単回経口投与したときの末梢血単核細胞のH-3アセチル化に対する作用を検討した。アセチル化誘導作用は25mg、32.5mgでは48時間、50mgでは24時間でそれぞれ最大に達した。
■ツシジノスタット単回経口投与後の末梢血単核細胞のH-3アセチル化に対する作用
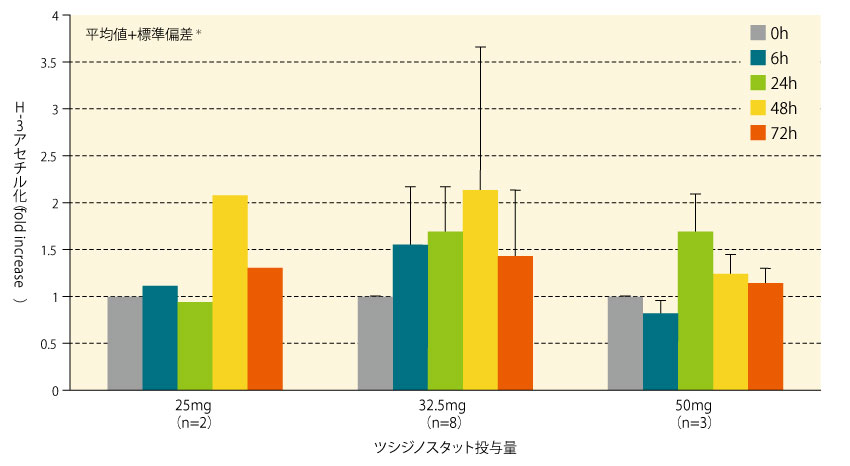
- *:25mg群は平均値のみ表示
- 方法:
- 固形がん又はリンパ腫を有する中国人患者13例に、ツシジノスタット25mg(2例)、32.5mg(8例)又は50mg(3例)を単回経口投与し、投与前、投与後6、24、48及び72時間の末梢血単核細胞におけるH-3アセチル化を検討した。
- 4. 効能又は効果
- 〇再発又は難治性の成人T細胞白血病リンパ腫
- 〇再発又は難治性の末梢性T細胞リンパ腫
- 6. 用法及び用量
- 通常、成人にはツシジノスタットとして1日1回40mgを週2回、3又は4日間隔で食後に経口投与する。
- なお、患者の状態により適宜減量する。
3. 非臨床薬理試験
-
(1)効力を裏付ける試験
1)HDAC酵素阻害(in vitro)22)
HDACアイソタイプ酵素阻害に対するツシジノスタットの選択性及び効力を検討したところ、ツシジノスタットはクラスⅠに属するHDAC1、HDAC2及びHDAC3、並びに、クラスⅡbに属するHDAC10を低濃度で阻害することが示され、その50%阻害濃度(IC50)は67~160nMであった。
■ツシジノスタットのHDAC酵素阻害(in vitro)
HDAC酵素 クラスⅠ クラスⅡa クラスⅡb クラスⅣ 1 2 3 8 4 5 7 9 6 10 11 IC50(μM) 0.095 0.160 0.067 0.733 >30 >30 >30 >30 >30 0.078 0.432 - 平均値(n=3)
Adapted with kind permission from Springer-Verlag: Cancer Chemother Pharmacol. 2012 Apr;69(4):901-9, Ning Z-Q, et al.
- 方法:
- ヒト組換えHDACタンパク質を用いて、ツシジノスタットのHDACアイソタイプ酵素に対するIC50値をin vitroで評価した。
2)H-3アセチル化に対する作用(in vitro、ex vivo)22)
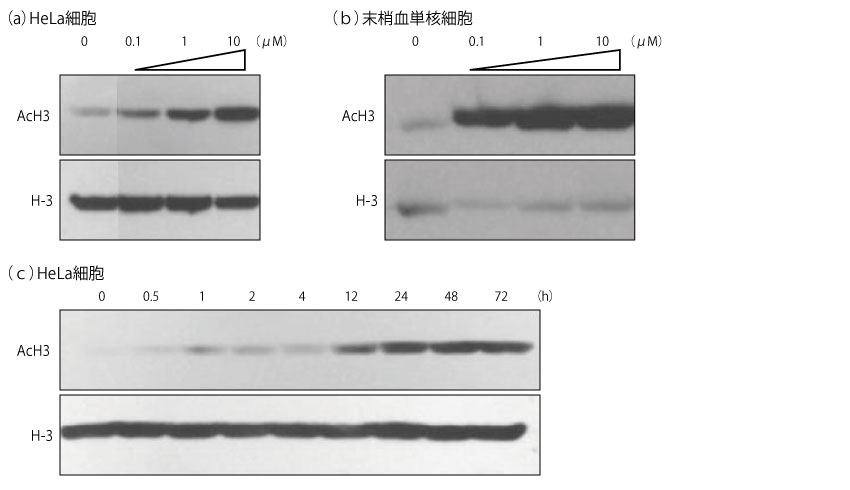
ヒト子宮頸部腺がんHeLa細胞及びヒト末梢血単核細胞を用いて、ツシジノスタットによるH-3アセチル化について検討したところ、いずれの細胞においても、ツシジノスタットによるアセチル化への誘導が示された(a、b)。
また、H-3アセチル化は、処理後0.5~1時間の時点で認められ、24~72時間で最大に達した(c)。■ヒトがん細胞及びヒト末梢血単核細胞におけるツシジノスタットのH-3アセチル化誘導(in vitro、ex vivo)
- Adapted with kind permission from Springer-Verlag: Cancer Chemother Pharmacol. 2012 Apr;69(4):901-9, Ning Z-Q, et al.
- 方法:
- (a)HeLa細胞を溶媒又はツシジノスタット0.1、1、10μMとともに24時間、(b)健常人から採取したヒト末梢血単核細胞を溶媒又はツシジノスタット0.1、1、10μMとともに24時間、(c)HeLa細胞をツシジノスタット1μMとともに0~72時間インキュベートした後、各細胞溶解物からヒストンを単離し、H-3アセチル化の状態を抗アセチル化H-3(AcH3)抗体及び再プローブした抗H-3抗体を用いたウェスタン免疫ブロット法により解析した。
- 21)Ning Z-Q, et al.: Cancer Chemother Pharmacol. 2012; 69(4): 901-9.Newman MJはHUYA Bioscience International, LLCに所属している。
3)がん細胞増殖抑制に対する作用(in vitro)22)
18種のヒト腫瘍由来細胞株を用いて、ツシジノスタットによる細胞増殖抑制に対する作用について検討した(n≧3)。
ツシジノスタットの50%増殖阻害濃度(GI50)は、卵巣がん、神経芽細胞腫及び胃がん由来細胞株を除く腫瘍細胞で低値を示した(GI50±標準誤差:急性T細胞白血病由来Jurkatで6.3±0.9、前骨髄球性白血病由来HL-60で0.4±0.1、バーキットリンパ腫由来Rajiで4.0±0.9、肝がん由来SMMC、HepG2でそれぞれ16±3.2、4.0±1.5)。
一方、ヒト胎児腎臓由来(CCC-HEK)及び肝臓由来(CCC-HEL)の正常細胞に対しての毒性は低く(GI50:ともに100超)、正常細胞とがん細胞では、ツシジノスタットに対する細胞毒性反応性は異なることが示唆された。- 方法:
- 18種のヒト腫瘍由来細胞株(A549、DU-145、LNCaP、MCF-7、MB-231、SK-OV-3、HeLa、SK-N-SH、HCT-8、SMMC、HepG2、PANC-1、SGC-7901、U2OS、Raji、HL-60、28SC、Jurkat)及び正常細胞(CCC-HEK、CCC-HEL)に、溶媒又はツシジノスタットを異なる濃度で添加し、処理後72時間の細胞生存率(溶媒と比較)について、CellTiter 96®AQueous One Solution Cell Proliferation Assayを用いて評価した。
4)<参考情報>ナチュラルキラー細胞を介した細胞障害性(ex vivo)22)
健常ドナーからの末梢血単核細胞を用いて、免疫系を介したツシジノスタットの抗腫瘍効果の潜在能力を検討した。ツシジノスタットによるナチュラルキラー(NK)細胞を介した細胞傷害性評価での標的細胞であるK562細胞の溶解作用は有意に高まり(a)、最大の標的細胞溶解活性はツシジノスタット100nMの添加時に認められ(b)、この濃度では48時間が最適培養時間であった(c)。K562細胞(標的細胞)のみにツシジノスタットを添加して培養したとき、ツシジノスタットを添加しなかった末梢血単核細胞(エフェクター細胞)の共存下で細胞溶解性は促進されなかったが、標的細胞及びエフェクター細胞の双方にツシジノスタットを添加したときには、エフェクター細胞のみに添加した場合と比較して細胞溶解性は有意に高まった(d)。
■ヒト骨髄性白血病由来K562細胞の免疫細胞を介した細胞溶解作用に対するツシジノスタットによる促進(ex vivo)
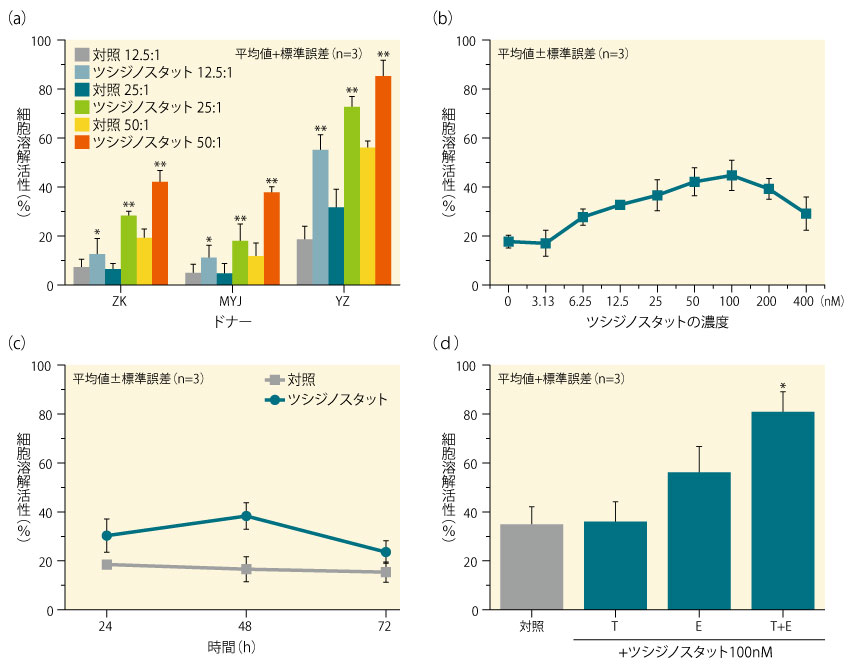
- *p<0.05、**p<0.01、スチューデントのt検定。
- T:標的細胞、E:エフェクター細胞、T+E:標的細胞とエフェクター細胞、E/T:標的細胞に対するエフェクター細胞の割合。
Adapted with kind permission from Springer-Verlag: Cancer Chemother Pharmacol. 2012 Apr;69(4):901-9, Ning Z-Q, et al.
- 方法:
- (a)健常ドナーから単離した末梢血単核細胞をツシジノスタット100nMで48時間処理し、次にE/T=12.5:1、25:1又は50:1でK562細胞とともに培養し、その後細胞毒性アッセイ(CytoTox 96® Non-Radioactive Cytotoxicity Assay)により評価した。p値はツシジノスタットで処理を行わなかった末梢血単核細胞の値との比較による。(b)末梢血単核細胞をツシジノスタット0~400nMで48時間処理した後、E/T=25:1で細胞毒性アッセイを行った。(c)末梢血単核細胞をツシジノスタット100nMで24~72時間処理した後、E/T=25:1で細胞毒性アッセイを行った。(d)ツシジノスタット100nMの存在下又は非存在下で48時間処理した後、E/T=25:1で細胞毒性アッセイを行った。
- 対照:
- 末梢血単核細胞、K562細胞ともにツシジノスタット非存在下で処理、T:K562細胞のみをツシジノスタットで処理、E:末梢血単核細胞のみをツシジノスタットで処理、T+E:末梢血単核細胞、K562細胞ともにツシジノスタットで処理。p値は末梢血単核細胞のみをツシジノスタットで処理したときの値との比較による。
免疫細胞を介した細胞溶解作用に関与することが知られているタンパク質パネルの発現レベルをフローサイトメトリーを用いて解析した。健常ドナー2例からの末梢血単核細胞にツシジノスタット100nMを添加して48時間後に、NK細胞の活性化に関与する受容体タンパク質であるCD16(低親和性免疫グロブリンG受容体)及びナチュラルキラーグループ2D(NKG2D)並びに細胞傷害性酵素であるグランザイムA(GZMA)の発現増加が認められた。
- 方法:
- 健常ドナー2例から単離した末梢血単核細胞をツシジノスタット100nMで48時間処理し、処理前と処理後のCD16、NKG2D及びGZMAの発現をフローサイトメトリーにより分析した。
- 22)Ning Z-Q, et al.: Cancer Chemother Pharmacol. 2012; 69(4): 901-9.Newman MJはHUYA Bioscience International, LLCに所属している。
5)抗腫瘍活性(in vitro、ex vivo)23)
①細胞生存能力の抑制(in vitro)23)
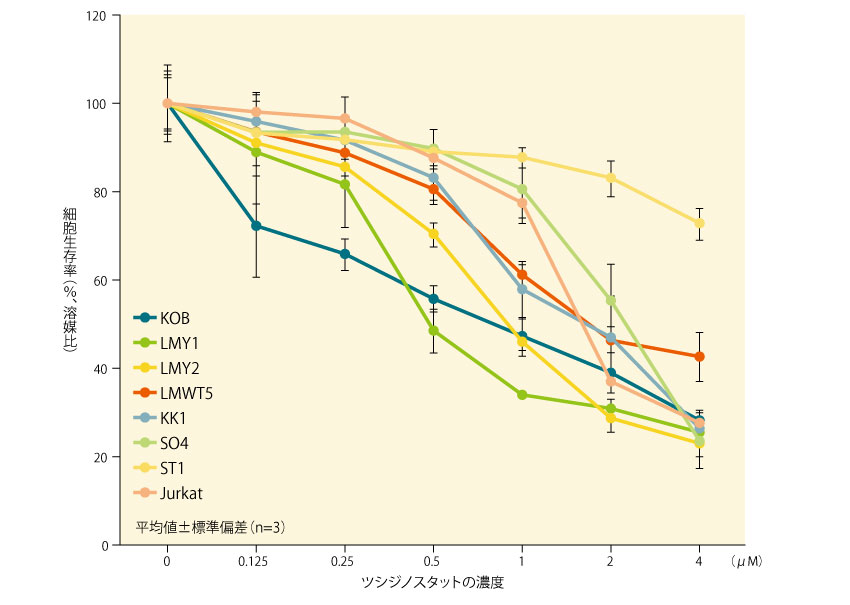
7種の初代ATL由来細胞株(KOB、LMY1、LMY2、LMWT5、KK1、SO4及びST1)、及びHDAC阻害剤が奏効することが知られているヒト急性T細胞白血病由来Jurkat株を用いて、ATL由来細胞株におけるツシジノスタットの活性を評価したところ、すべての細胞株で細胞の生存能力の低下が示された。
また、Jurkatは非ATL由来細胞であること、Jurkat及びST1ではIL-2が添加されていないこと、KOB、LMY1、LMY2及びST1は野生型がん抑制タンパク質p53を保持している細胞株であることなどから、HTLV-1感染、IL-2依存性及びp53遺伝子発現の有無はツシジノスタットへの反応に影響を及ぼさないことが示唆された。■初代ATL由来細胞株におけるツシジノスタットの細胞生存能力の抑制(in vitro)
- Induction of apoptosis by HBI‐8000 in adult T‐cell leukemia/lymphoma is associated with activation of Bim and NLRP3,
- Hasegawa H, et al. Cancer Sci. 2016 Aug;107(8):1124-33. © 2016 The Authors. Cancer Science published by John Wiley & Sons Australia, Ltd
- on behalf of Japanese Cancer Association. Reproduced with permission of John Wiley and Sons, Inc.
- 方法:
- 7種の初代ATL由来細胞株及びJurkat細胞を溶媒又はツシジノスタット0.125~4μMで処理し、処理後72時間の細胞生存率(溶媒と比較)について、MTSアッセイ[5(- 3-カルボメトキシフェニル)-2(- 4,5-ジメチル-チアゾイル)-3-(4-スルフォフェニル)テトラゾリウムアッセイ]を用いて評価した。なお、Jurkat及びST1以外にはIL-2を添加した。
②細胞生存能力の抑制(ex vivo)23)
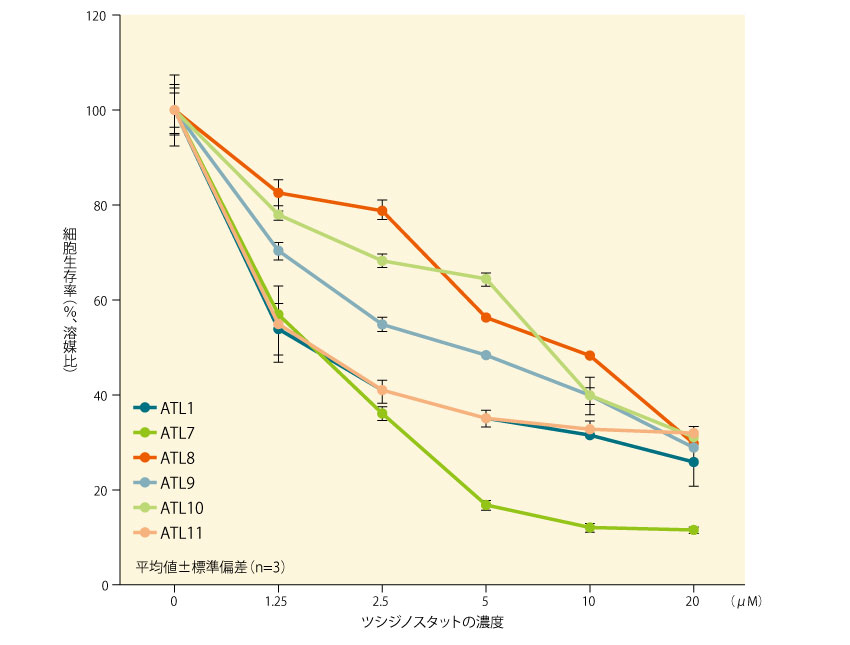
ATL患者10例から採取した11種の初代ATL細胞のうち、再発2例(ATL1及びATL10)、及び予後不良因子を有する慢性型2例(ATL7及びATL8)を含む6種の初代ATL細胞を用いて、ATL細胞におけるツシジノスタットの活性を検討したところ、すべての細胞において用量依存的な生存能力の低下が示された。
■初代ATL細胞におけるツシジノスタットの細胞生存能力の抑制(ex vivo)
- Induction of apoptosis by HBI‐8000 in adult T‐cell leukemia/lymphoma is associated with activation of Bim and NLRP3,
- Hasegawa H, et al. Cancer Sci. 2016 Aug;107(8):1124-33. © 2016 The Authors. Cancer Science published by John Wiley & Sons Australia, Ltd
- on behalf of Japanese Cancer Association. Reproduced with permission of John Wiley and Sons, Inc.
- 方法:
- ATL患者10例から採取した11種の初代ATL細胞のうち、再発2例(ATL1及びATL10)、及び予後不良因子を有する慢性型2例(ATL7及びATL8)を含む6種の初代ATL細胞を溶媒又はツシジノスタット1.25~20μMで処理し、処理後72時間の細胞生存率(溶媒と比較)について、MTSアッセイを用いて評価した。
-
- 23)Hasegawa H, et al.: Cancer Sci. 2016; 107(8): 1124-33.
- Hasegawa HはHUYA Bioscience International, LLCから研究費を受領している。
- Bissonnette RPはHUYA Bioscience International, LLCの社員である。
- Gillings MはHUYA Bioscience International, LLCで役職に就いている。
③アポトーシスの誘導(in vitro)23)
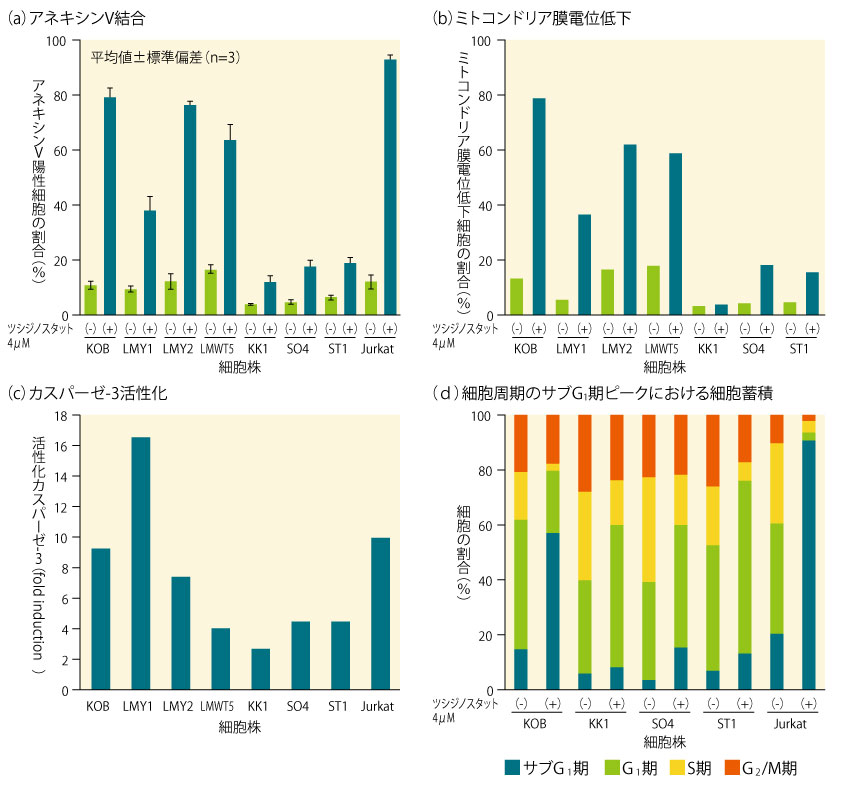
7種の初代ATL由来細胞株(KOB、LMY1、LMY2、LMWT5、KK1、SO4及びST1)、及びヒト急性T細胞白血病由来Jurkat株における、ツシジノスタットによるアポトーシスの誘導について、4つのアッセイを用いて評価した。
その結果、(a)アネキシンV結合、(b)ミトコンドリア膜電位低下、(c)カスパーゼ-3活性化のいずれにおいても、KOB、LMY1、LMY2、LMWT5及びJurkatで、ツシジノスタットによるアポトーシスの誘導が示された。
また、(d)細胞周期においては、KK1、SO4及びST1で、ツシジノスタットによるG1期での細胞周期停止の誘導が認められた。■初代ATL由来細胞株におけるツシジノスタットによるアポトーシス誘導(in vitro)
- Induction of apoptosis by HBI‐8000 in adult T‐cell leukemia/lymphoma is associated with activation of Bim and NLRP3,
- Hasegawa H, et al. Cancer Sci. 2016 Aug;107(8):1124-33. © 2016 The Authors. Cancer Science published by John Wiley & Sons Australia, Ltd
- on behalf of Japanese Cancer Association. Reproduced with permission of John Wiley and Sons, Inc.
- 方法:
- 7種の初代ATL由来細胞株及びJurkat細胞を溶媒又はツシジノスタット4μMで48時間処理した後、(a)~(d)のアッセイを用いて、アポトーシス誘導の測定を行った。(a)アネキシンV/ヨウ化プロピジウム染色を行い、アネキシンV陽性細胞の割合を評価した。(b)細胞をJC-1色素とともにインキュベートし、フローサイトメトリーで分析することにより、JC-1赤色蛍光強度の低い細胞の割合を求め、ミトコンドリア膜電位の低下を評価した。(c)活性化された(切断された)カスパーゼ-3をAPOPCYTETM caspase-3 colorimetric assay kitにより評価した。fold induction:ツシジノスタット処置細胞/ツシジノスタット未処置細胞。(d)Cell Cycle Test ki(t BD Bioscience, San Jose, CA, USA)を用いて細胞周期を評価し、各相にある細胞の割合を算出した。
④アポトーシスの誘導(ex vivo)23)
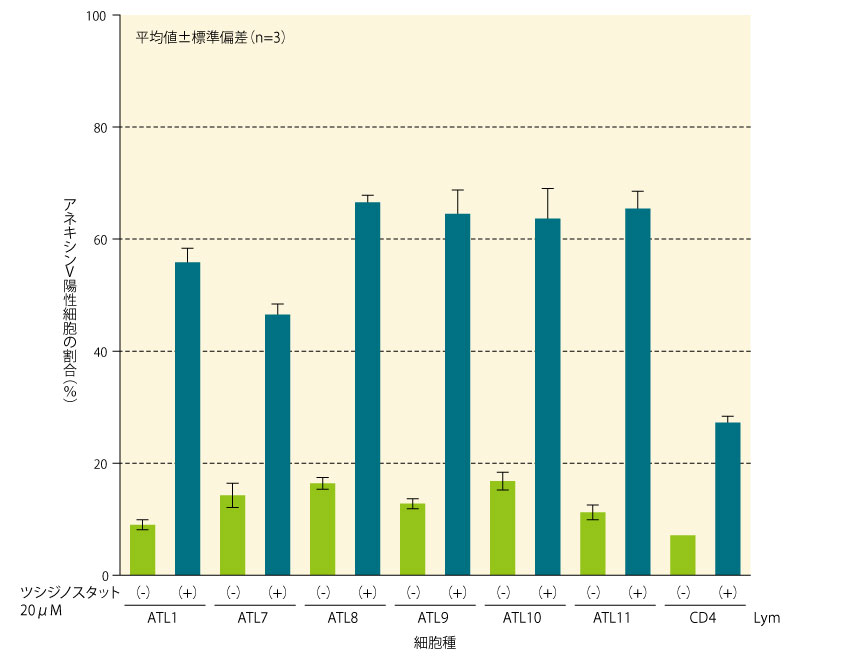
ATL患者10例から採取した11種の初代ATL細胞のうち、再発2例(ATL1及びATL10)、及び予後不良因子を有する慢性型2例(ATL7及びATL8)を含む6種の初代ATL細胞における、ツシジノスタットによるアポトーシスの誘導について、アネキシンV/ヨウ化プロピジウムアッセイを用いて評価した。
すべてのATL細胞において、アネキシンV陽性細胞の割合が50%超であったことから、ツシジノスタットは初代ATL細胞においてアポトーシスによる細胞死を誘導したことが示された。なお、対照であるCD4陽性細胞におけるアネキシンV陽性細胞の割合は30%未満であった。■初代ATL細胞におけるツシジノスタットによるアポトーシス誘導(ex vivo)
- Induction of apoptosis by HBI‐8000 in adult T‐cell leukemia/lymphoma is associated with activation of Bim and NLRP3,
- Hasegawa H, et al. Cancer Sci. 2016 Aug;107(8):1124-33. © 2016 The Authors. Cancer Science published by John Wiley & Sons Australia, Ltd
- on behalf of Japanese Cancer Association. Reproduced with permission of John Wiley and Sons, Inc.
- 方法:
- ATL患者10例から採取した11種の初代ATL細胞のうち、再発2例(ATL1及びATL10)、及び予後不良因子を有する慢性型2例(ATL7及びATL8)を含む6種の初代ATL細胞及び正常CD4陽性細胞を溶媒又はツシジノスタット20μMで48時間処理した後、アネキシンV/ヨウ化プロピジウム染色を行い、アネキシンV陽性細胞の割合を評価した。
-
- 23)Hasegawa H, et al.: Cancer Sci. 2016; 107(8): 1124-33.
- Hasegawa HはHUYA Bioscience International, LLCから研究費を受領している。
- Bissonnette RPはHUYA Bioscience International, LLCの社員である。
- Gillings MはHUYA Bioscience International, LLCで役職に就いている。
閲覧履歴
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。


 くすりに関する
くすりに関する