ハイヤスタ錠 薬物動態
薬物動態
1. 血漿中濃度
-
(1)単回及び反復投与(日本人NHL患者)8)
日本人NHL患者にツシジノスタット30mg又は40mgを朝食後に週2回、3又は4日間隔で経口投与したとき、投与1日目(単回投与)及び25日目(反復投与)の血漿中ツシジノスタット濃度推移及び薬物動態パラメータは以下の通りであった。
血漿中ツシジノスタット濃度は、投与量及び投与回数にかかわらず、投与後3~6時間でCmaxに到達し、t1/2は17~22時間であった。また、反復投与時のAUC0-tau及びCmaxの累積係数(RAUC0-tau及びRCmax)に基づく蓄積は、116%~127%であった。■ツシジノスタット30mg又は40mg単回及び反復経口投与時の血漿中ツシジノスタット濃度推移
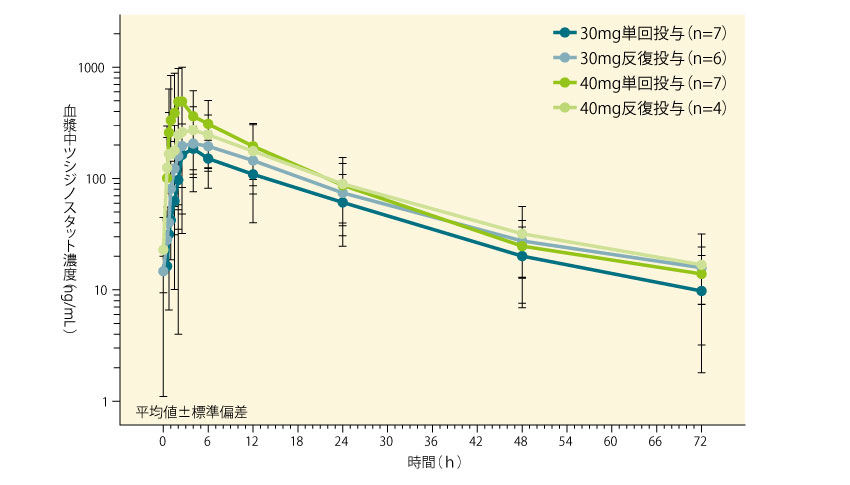
■ツシジノスタット30mg又は40mg単回及び反復経口投与時のツシジノスタットの薬物動態パラメータ
薬物動態パラメータ ツシジノスタット30mg ツシジノスタット40mg 投与1日目(単回)(n=7) 投与25日目(反復)(n=6) 投与1日目(単回)(n=7) 投与25日目(反復)(n=4) tmax(h) 3.98*
[2.50, 11.9]5.00*
[2.47, 12.0]2.42*
[1.52, 5.95]4.19*
[0.78, 12.0]Cmax(ng/mL) 199±105
[93.3, 405]240±79.6
[153, 318]590±464
[123, 1440]385±218
[84.0, 581]t1/2(h) 17.1±3.15
[12.9, 21.2]21.6±5.27
[14.4, 29.2]19.4±6.51
[12.5, 32.1]18.7±2.05
[16.5, 21.2]AUC0-tau(ng・h/mL) 3740±1210
[2210, 5280]4870±1320
[3070, 6250]6760±3650
[2070, 13700]6010±3500
[2270, 10700]RAUC0-tau(%) - 123(8.8)
[111, 139]- 124(38.5)
[69.7, 184]RCmax(%) - 116(23.8)
[78.5, 165]- 127(44.0)
[68.3, 176]- 平均値±標準偏差、[最小, 最大]、(変動係数 %)、*:中央値、tmax:最高血漿中濃度到達時間、Cmax:最高血漿中濃度、t1/2:消失半減期、AUC0-tau:0時点から次投与までの血漿中濃度-時間曲線下面積、RAUC0-tau:投与25日目のAUC0-tau/投与1日目のAUC0-tauの比(%)、RCmax:投与25日目のCmax/投与1日目のCmaxの比(%)
- 対象:
- 日本人NHL患者14例
- 方法:
- ツシジノスタット30mg又は40mgを朝食後に週2回、3又は4日間隔で経口投与し、投与1日目及び25日目の薬物動態を検討した。
- 4. 効能又は効果
- 〇再発又は難治性の成人T細胞白血病リンパ腫
- 〇再発又は難治性の末梢性T細胞リンパ腫
- 6. 用法及び用量
- 通常、成人にはツシジノスタットとして1日1回40mgを週2回、3又は4日間隔で食後に経口投与する。
- なお、患者の状態により適宜減量する。
-
(2)食事の影響(外国人データ)9)
米国人健康成人16例に、ツシジノスタット20mgを食後*30分又は絶食下で単回経口投与したとき、食後及び絶食下の薬物動態パラメータは以下の通りであった。
血漿中ツシジノスタット濃度は、食後投与では絶食下投与に比べて、tmaxの遅延と低値のCmaxを示したが、tmax以降は投与後72時間まで高値で推移した。絶食下投与に対する食後投与におけるCmax及びAUCinfの幾何平均値の比(90%CI)は、それぞれ0.757(0.615, 0.932)及び1.094(0.968, 1.237)であった。- *:高脂肪食(総カロリー約800~1,000kcalのうち脂質50%)摂取
■食後又は絶食下におけるツシジノスタット20mg単回経口投与時のツシジノスタットの薬物動態パラメータ
薬物動態パラメータ 食後投与(n=16) 絶食下投与(n=16) tmax(h) 4.5(2.0, 8.0)*1 2.0(1.0, 4.0)*1 Cmax(ng/mL) 104.48(38.0) 137.93(43.4) t1/2(h) 19.33(45.0) 24.25(41.5)*2 AUClast(ng・h/mL) 1502.0(27.9) 1366.4(31.9) AUCinf(ng・h/mL) 1605.9(26.2) 1417.9(29.5)*2 - 幾何平均値(幾何変動係数 %)
- AUClast:0時点から最終検出時点までの血漿中濃度-時間曲線下面積、AUCinf:0時点から無限大時間までの血漿中濃度-時間曲線下面積
- *1:中央値(最小, 最大)、*2:n=15
- 対象:
- 米国人健康成人16例
- 方法:
- ツシジノスタット(予定されている市販製剤と同じ製剤)20mgを食後*30分又は絶食下で単回経口投与し、交叉試験法により、食後及び絶食下における薬物動態を検討した。
- *:高脂肪食(総カロリー約800~1,000kcalのうち脂質50%)摂取
- 4. 効能又は効果
- 〇再発又は難治性の成人T細胞白血病リンパ腫
- 〇再発又は難治性の末梢性T細胞リンパ腫
- 6. 用法及び用量
- 通常、成人にはツシジノスタットとして1日1回40mgを週2回、3又は4日間隔で食後に経口投与する。
- なお、患者の状態により適宜減量する。
-
(3)腎機能障害患者における薬物動態(母集団薬物動態解析、一部外国人データ)10)
固形がん又は血液がんを有する患者を対象とした母集団薬物動態解析における、対象集団の腎機能障害の程度は、正常患者[クレアチニンクリアランス(CRCL)≧90mL/分]20例、軽度腎機能障害患者(90mL/分>CRCL≧60mL/分)29例、中等度腎機能障害患者(60mL/分>CRCL≧30mL/分)16例であった。
母集団薬物動態解析では、CRCLの低下に伴い曝露量が上昇する傾向が認められた。
母集団薬物動態解析におけるCRCL中央値(76mL/分)の標準患者に対して、CRCL 43mL/分(5パーセンタイル値)又は125mL/分(95パーセンタイル値)の患者における曝露量変動は25%以内と推定された。
腎機能障害の程度と見かけのクリアランス(CL/F)及び定常状態下の曝露量(AUCss)との関連性を検討した結果は下図の通りで、腎機能障害の重症度に伴うCL/Fの減少とAUCssの増加が示された。■ツシジノスタットの見かけのクリアランス及び定常状態下AUCに対する腎機能障害の影響
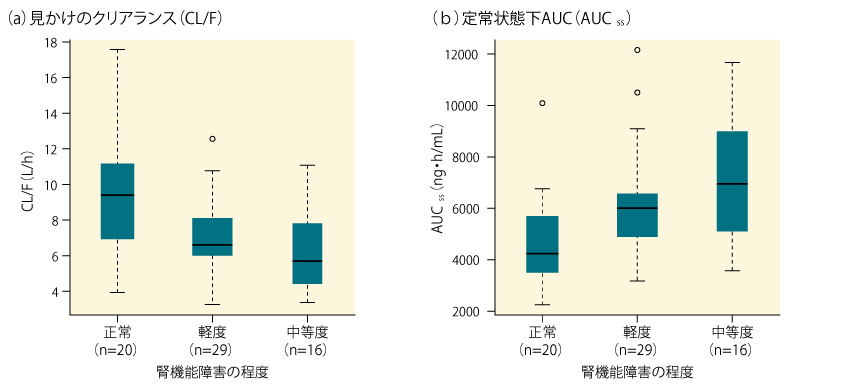
- 箱ひげ図は、上から75%四分位、中央値、25%四分位を示し、バーの上段が95%分位点、下段が5%分位点を示す。
- 方法:
- 固形がん又は血液がんを有する患者を対象とした臨床試験、すなわち国内第Ⅰ相試験、国際共同第Ⅱb相試験及び海外第Ⅰb/Ⅱ相試験における血漿中ツシジノスタット濃度データ(65例、1052点)を用いて、母集団薬物動態解析を実施した。
国内第Ⅰ相試験(HBI-8000-201試験):日本人NHL患者14例を対象として、ツシジノスタット30mg(7例)又は40mg(7例)を食後に単回投与したときの薬物動態を検討した。
国際共同第Ⅱb相試験(HBI-8000-203試験):再発又は難治性のPTCL患者26例(日本人10例、韓国人16例)を対象として、ツシジノスタット40mgを食後に単回投与したときの薬物動態を検討した。
海外第Ⅰb/Ⅱ相試験(HBI-8000-302試験):米国人固形がん患者25例を対象として、ツシジノスタット20mg(3例)、30mg(15例)又は40mg(7例)を食後に単回投与したときの薬物動態を検討した。
-
(4)高齢患者における薬物動態(母集団薬物動態解析、一部外国人データ)10)
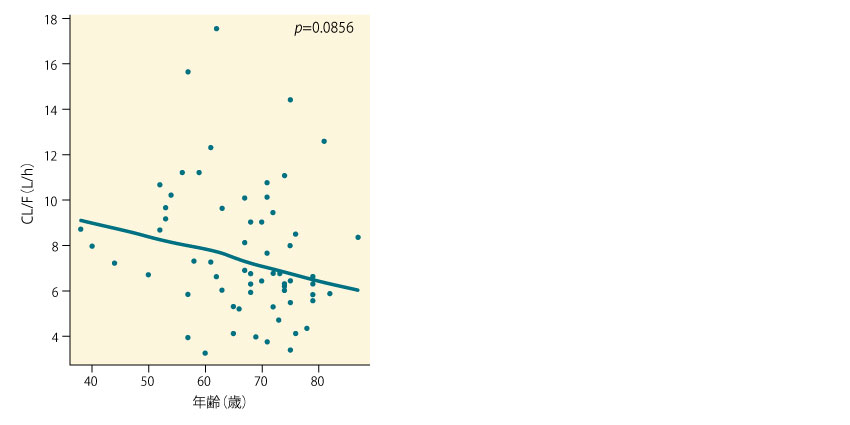
母集団薬物動態解析における、CL/Fと年齢の関連性は、下図の通りであった。加齢に伴うCL/Fの低下傾向が認められたが、この関連性に有意差は認められなかった(p>0.05、直線回帰分析)。
■ツシジノスタットのCL/Fと年齢との関連性
- 方法:
- 固形がん又は血液がんを有する患者を対象とした国内第Ⅰ相試験、国際共同第Ⅱb相試験及び海外第Ⅰb/Ⅱ相試験における血漿中ツシジノスタット濃度データ(65例、1052点)を用いて、母集団薬物動態解析を実施した。
- 4. 効能又は効果
- 〇再発又は難治性の成人T細胞白血病リンパ腫
- 〇再発又は難治性の末梢性T細胞リンパ腫
- 6. 用法及び用量
- 通常、成人にはツシジノスタットとして1日1回40mgを週2回、3又は4日間隔で食後に経口投与する。
- なお、患者の状態により適宜減量する。
-
(5)QT/QTcFに及ぼす影響(外国人データ)11)
固形がんを有する米国人患者14例に、ツシジノスタット20mg、30mg又は40mgを単回投与したときのQT/QTcFに対する影響を検討したところ、いずれの用量においてもQTcFが450msec以下、ΔQTcFが30msec以下であった。また、血漿中ツシジノスタット濃度の上昇に伴う、ΔQTcF変化量の低下が認められた。ΔQTcF平均変化量の90%CIの上限は、用量を通じて-1.1~-2.8msecであり、重要な影響とみなす閾値である10msecを下回る値であった。
■ツシジノスタット単回経口投与後の最大濃度時点におけるΔQTcFの平均変化量の推定値
ツシジノスタット投与量 患者数/観察数 Cmax(幾何平均)(ng/mL) ΔQTcFの平均変化(msec) 90%CI 20mg 1/5 104.9 -2.259 -3.373, -1.145 30mg 6/30 117.6 -2.533 -3.782, -1.284 40mg 7/32 259.3 -5.584 -8.339, -2.830 - すべての測定時点をモデルに組み入れた。定量限界未満の値は0とした。
- 対象:
- 固形がんを有する米国人患者14例
- 方法:
- 対象に、ツシジノスタット20mg(1例)、30mg(6例)又は40mg(7例)を朝食後に単回経口投与し、朝食1時間以上前から投与後4時間にわたり12誘導ホルター心電図モニタリングを行った。
Fridericiaの補正式を用いたQT間隔(QTcF)及び投与直前からのQTcFの変化量(ΔQTcF)を計測し、ツシジノスタットのQT/QTcFに及ぼす影響を検討した。
8. 重要な基本的注意(抜粋)
8.3 QT間隔延長、不整脈等があらわれることがあるので、本剤の投与開始前及び投与中に、必要に応じて心機能検査(心電図、心エコー検査等)及び電解質検査(カリウム、カルシウム等)を行い、患者の状態を十分に確認すること。また、必要に応じて、電解質(カリウム、カルシウム等)を補正すること。[9.1.2、9.1.3、11.1.4 参照]
9. 特定の背景を有する患者に関する注意(抜粋)
9.1 合併症・既往歴等のある患者
- 9.1.3 QT間隔延長又はその既往歴のある患者
- QT間隔延長を起こすおそれがある。[8.3、11.1.4参照]
10. 相互作用(抜粋)
- 10.2 併用注意(併用に注意すること)(抜粋)
-
- 薬剤名等:
- 抗不整脈薬 アミオダロン、ジソピラミド、プロカインアミド等
QT間隔を延長させることが知られている他の薬剤 クラリスロマイシン、モキシフロキサシン、ベプリジル等
- 臨床症状・措置方法:
- QT間隔延長を増強するおそれがあるため、併用を避けることが望ましい。
併用する場合には、患者の状態をより慎重に観察すること。
- 機序・危険因子:
- これらの薬剤ではQT間隔を延長するとの報告があり、相加的なQT間隔延長を起こすことがある。
2. 分布
-
(1)血漿蛋白結合率(in vitro)12)
ヒト、Sprague-Dawley系ラット及びビーグル犬の血漿を用いて、ツシジノスタットの血漿蛋白結合を、超遠心法で検討したところ、0.3~3μMの濃度範囲におけるツシジノスタットの結合率は、ヒトで88.9%~89.4%、ラットで86.4%~87.9%、イヌで79.1%~80.1%であった。
-
(2)血球移行性(in vitro)13)
ヒト、Sprague-Dawley系ラット及びビーグル犬の全血を用いて、ツシジノスタットの赤血球への移行性について検討したところ、0.168~1.68μMの濃度範囲におけるツシジノスタットの血球への平均分配率(全血/血漿濃度比)は、ヒトで59.2%~76.0%、ラットで48.1%~52.8%、イヌで52.5%~57.8%であった。また、ヒトでの血球分配率は濃度の上昇につれて低下した。
-
(3)組織内分布(ラット)14)
部分有色ラット(Long Evans系、雄9匹)に、14C-ツシジノスタットを9mg/kgで単回経口投与し、投与後2、8、24、48、72、120、168、336及び840時間の組織中放射能濃度を測定した。
高濃度の放射能が認められた組織は副腎及び腎臓で、比較的高濃度の放射能が認められた組織は膀胱壁、肝臓、下垂体、脾臓、ハーダー腺及び大動脈であった(消化管内容物を除く)。
放射能は、投与後2時間で大部分の組織に認められたが、大腸内容物、脳/脊髄、骨、白色脂肪及び水晶体では定量下限未満であった。
組織内放射能は、大部分の組織において、投与後2~8時間で最高濃度に達した。投与後8時間以降に最高濃度に達した組織(消化管内容物を除く)は、下垂体、ブドウ膜、ハーダー腺、リンパ節、脾臓、胸腺及び膀胱内容物であった。
ブドウ膜では、投与後24時間に最高濃度に達し、最終採取時の840時間まで残存したことから、ツシジノスタット由来成分のメラニン親和性が示された。
ブドウ膜を除くすべての組織において、組織内放射能は投与後24時間には減少が認められ、投与後120時間までには定量下限未満となった。
循環血では、放射能濃度は大部分の組織より低く推移し、投与後24時間までに定量下限未満となった。
脳及び脊髄では、放射能濃度が定量下限未満で推移したことから、ツシジノスタットは血液脳関門を通過しないことが示された。
3. 代謝(in vitro)15),16)
ヒト肝ミクロソーム、ヒト及びラット肝細胞を用いたin vitro試験において、ツシジノスタットは主にCYP3A4による代謝を受けることが示され、代謝物として、酸化体及び脱アルキル化体の3つの第Ⅰ相代謝物が検出された。また、ツシジノスタットの代謝は、還元型ニコチンアミドジヌクレオチドリン酸(NADPH)非存在下で安定していることが示唆され、ツシジノスタットの11%~41%がNADPH存在下で代謝を受けるものと考えられた。
■ツシジノスタットの推定代謝経路
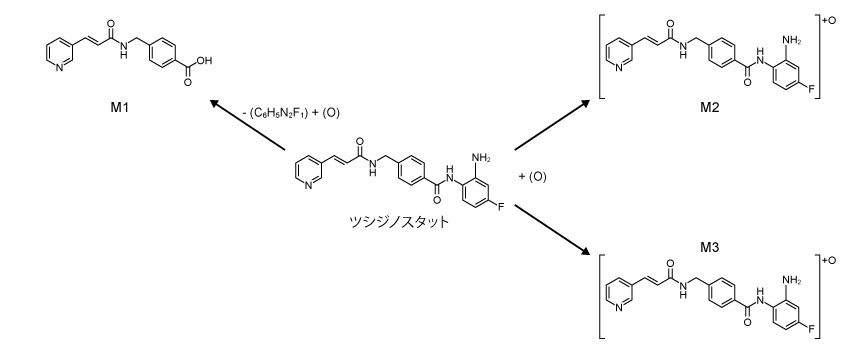
4. 排泄(日本人NHL患者)8)
日本人NHL患者にツシジノスタット40mgを朝食後単回経口投与し、投与後72時間の尿中回収率について検討したところ、総投与量の25.2%が投与後72時間までに未変化体として尿中に排泄された。
5. 薬物相互作用
-
(1)イトラコナゾール(外国人データ)17)
米国人健康成人16例を対象とした試験でイトラコナゾール(強いCYP3A阻害剤)が投与された15例では、イトラコナゾール200mgを1日1回反復経口投与し、ツシジノスタット20mgを単回経口投与した。ツシジノスタット単独投与時に対するイトラコナゾール併用投与時における本剤のCmax及びAUCinfの幾何平均値の比(90%CI)は、それぞれ1.41(1.02, 1.94)及び1.46(1.23, 1.72)であった。
-
(2)CYP阻害剤(in vitro)15),16),18),19)
in vitro試験において、ツシジノスタットはCYP3A4の基質であり、CYP3A4による代謝を受けること14), 15)、またCYP阻害試験において、主にCYP3A4を阻害すること17), 18)が報告されている。
-
(3)CYP誘導剤(in vitro)19),20)
CYP誘導試験において、ツシジノスタットはCYP3A4の軽度の誘導作用を有することが示唆された。
-
(4)トランスポーター阻害剤(in vitro)19),21)
トランスポーター阻害試験において、ツシジノスタットは、MATE2-Kを軽度阻害することが報告されている。また、トランスポーター基質性試験において、いくつかの取り込みトランスポーター(OAT3及びMATE2-K)及び排出トランスポーター(P-gp、BCRP及びMRP2)の基質となることが報告されている。
- 4. 効能又は効果
- 〇再発又は難治性の成人T細胞白血病リンパ腫
- 〇再発又は難治性の末梢性T細胞リンパ腫
- 6. 用法及び用量
- 通常、成人にはツシジノスタットとして1日1回40mgを週2回、3又は4日間隔で食後に経口投与する。
- なお、患者の状態により適宜減量する。
10. 相互作用(抜粋)
- 10.2 併用注意(併用に注意すること)(抜粋)
-
- 薬剤名等:
- 強いCYP3A阻害剤 イトラコナゾール、ボリコナゾール、クラリスロマイシン等グレープフルーツ含有食品[16.7.1参照]
- 臨床症状・措置方法:
- 本剤の副作用が増強されるおそれがあるので、併用する場合には、本剤の減量を考慮するとともに、患者の状態をより慎重に観察し、副作用の発現に十分注意すること。
- 機序・危険因子:
- これらの薬剤等の強いCYP3A阻害作用により、本剤の代謝が阻害され、本剤の血中濃度が上昇する可能性がある。
閲覧履歴
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。


 くすりに関する
くすりに関する