ハイヤスタ錠 臨床成績 再発又は難治性の末梢性T細胞リンパ腫(PTCL)
臨床成績 再発又は難治性の末梢性T細胞リンパ腫(PTCL)
日本人及び韓国人PTCL患者を対象とする国際共同第Ⅱb相試験(HBI-8000-203試験)6),7)
社内資料:国際共同第Ⅱb相試験(HBI-8000-203試験)(承認時評価資料)
Rai S, et al.: Haematologica. 2024 Jun 6. doi: 10.3324/haematol.2023.283992.
著者にMeiji Seika ファルマから謝礼等を受領している者が含まれる。
著者にHUYABIO Internationalから研究費等を受領している者及び同社の社員が含まれる。
試験概要
- 目的:
- 再発又は難治性PTCL※1を有する日本人及び韓国人患者を対象に、ハイヤスタを4週間のサイクルで週2回経口投与したときの有効性※2及び安全性を検討する。
- 対象:
-
抗がん剤による全身療法を1レジメン以上施行し、他の標準的治療法が適さない再発又は難治性PTCLを有する日本人又は韓国人患者55例(日本人39例)
FAS:49例
PPS:46例
SAF:55例
【主な組み入れ基準】- 組織学的又は細胞学的にPTCLと診断された患者[WHO分類(2008)に基づく]
- 評価可能病変が1つ以上認められる患者
- ECOG PSが0~2である患者
- 余命が3ヵ月超と判断された患者
- 臓器移植を受けていない患者
- 同種幹細胞移植を受けていない患者
- 治験薬投与開始前12週間以内に自家幹細胞移植を受けていない患者
- 活動性感染症がない患者
- 心臓の異常又は不整脈を有さない患者
- 試験デザイン:
- 多施設共同・非盲検・非無作為化・単一群試験
- 方法:
- 対象患者にハイヤスタ40mgを食後(約30分後)に週2回(投与間隔3~4日)経口投与し、投与サイクルは1サイクルあたり4週間とした。
- 治療期間:
- PD又は適切な本薬の休薬もしくは減量にもかかわらず許容できない毒性のいずれかが最初に認められるまで。
- 評価項目:
-
- 主要評価項目(検証的な解析結果):
- ORR※3(IOERC評価)
- 副次評価項目:
- PTCL病理組織型別ORR[サブグループ解析]、PFSの中央値(IOERC評価)、DORの中央値(IOERC評価)
- 探索的評価項目:
- OS、薬物動態※4、DCR※5、TTR※6、腫瘍縮小効果(標的病変の総腫瘍サイズのベースラインからの最大変化、皮膚病変のmSWATスコア)、部分集団別ORR[サブグループ解析]、部分集団別PFS[サブグループ解析]、部分集団別OS[サブグループ解析]等
- 安全性評価項目:
- 有害事象等(MedDRA ver.21.1、NCI-CTCAE ver.4.03)
- 解析計画:
- 安全性及び有効性のすべてのパラメータは、記述統計を用いて解析した。カテゴリー変数は度数分布(被験者数及び割合)を用いて要約した。連続変数は平均値、標準偏差、中央値、最小値及び最大値を用いて要約した。Time-to-event型変数はKaplan-Meier法及びKaplan-Meier曲線の図示による中央値の推定を用いて要約した。主要評価項目である有効性の解析は、IOERC及びIRRによる評価に基づきPPSを対象とし、ORRは正確な二項分布の95%CIで要約した。
サブグループ解析として、国別、性別、年齢、ECOG PS、PTCL病理組織型、PTCLサブセット、前治療レジメン数、直近のがん治療からの期間の評価が事前規定された。CIの下限値が10%の閾値より高い場合、ORRは10%より有意に優れていると結論付けた。本治験の目標ORRを30%とした。なお、一次解析はカットオフ日(最終被験者の2回目の有効性評価完了時点)までのデータを基に解析した。
- 試験期間:
- 2017年3月から2018年11月までに計74例の患者が登録され、うち55例がハイヤスタを投与された。2022年2月に試験が終了した。(データカットオフ:一次解析 2019年3月、最終解析 2022年2月)
- ※1:対象患者の病理組織型;PTCL・非特定型(PTCL-NOS)、血管免疫芽球性T細胞リンパ腫(AITL)、未分化リンパ腫キナーゼ(ALK)陰性未分化大細胞リンパ腫(ALCL ALK-)、腸管症関連T細胞リンパ腫(EATL)、肝脾T細胞リンパ腫(HSTCL)、皮下脂肪織炎様T細胞リンパ腫(SPTCL)、ALK陽性ALCL(ALCL ALK+)
- ※2:治療効果及びPTCLのPDは、リンパ腫における治療効果判定基準改訂版(Cheson 2014)に従って評価し、皮膚病変は、mSWAT(Stevens 2002、Olsen 2011)に従って評価した
- ※3:CR又はPRが認められた患者の割合
- ※4:特定の治験実施医療機関のみ
- ※5:CR、PR又はSDが認められた患者の割合
- ※6:初回投与からPR以上の効果が認められるまでの期間
有効性(一次解析結果)
-
(1)客観的奏効率(ORR)(IOERC評価、PPS)〔主要評価項目、検証的な解析結果〕
IOERC評価によるORR及び最良総合効果は下表の通りであった。
主要評価項目であるPPSのORRは45.7%(21/46例、95%C:I 30.9, 61.0)であり、本試験の目標である30%を超え、95%CIの下限が本試験で規定した10%の閾値を上回っていた。■ORR及び最良総合効果(IOERC評価、PPS)〔主要評価項目〕
例数
NCR
n(%)PR
n(%)SD
n(%)PD
n(%)〔主要評価項目〕 ORR
n/N(%)95%CI PPS 46 5
(10.9)16
(34.8)12
(26.1)13
(28.3)21/46
(45.7)30.9, 61.0 - n/N:該当する被験者数/解析対象集団の被験者数
-
(2)PTCL病理組織型別客観的奏効率(ORR)(IOERC評価、PPS)〔副次評価項目〕[サブグループ解析]
CPRによって確認されたPTCL病理組織型は、PTCL-NOSが34例、AITLが8例、ALCL ALK-が3例、EATLが1例であった。ALCL ALK+、HSTCL及びSPTCLの被験者はいなかった。副次評価項目であるPPSのPTCL病理組織型別ORR及び最良総合効果は下表の通りであった。
■CPRによるPTCL病理組織型別ORR及び最良総合効果(IOERC評価、PPS)〔副次評価項目〕
例数
NCR
n(%)PR
n(%)SD
n(%)PD
n(%)〔副次評価項目〕 ORR
n/N(%)95%CI PTCL-NOS 34 3
(8.8)9
(26.5)10
(29.4)12
(35.3)12/34
(35.3)19.7, 53.5 AITL 8 2 5 1 0 7/8 - ALCL ALK- 3 0 1 1 1 1/3 - EATL 1 0 1 0 0 1/1 - - n/N:該当する被験者数/PTCL病理組織型別の被験者数
-
(3)無増悪生存期間(PFS)の中央値(IOERC評価、PPS)〔副次評価項目〕
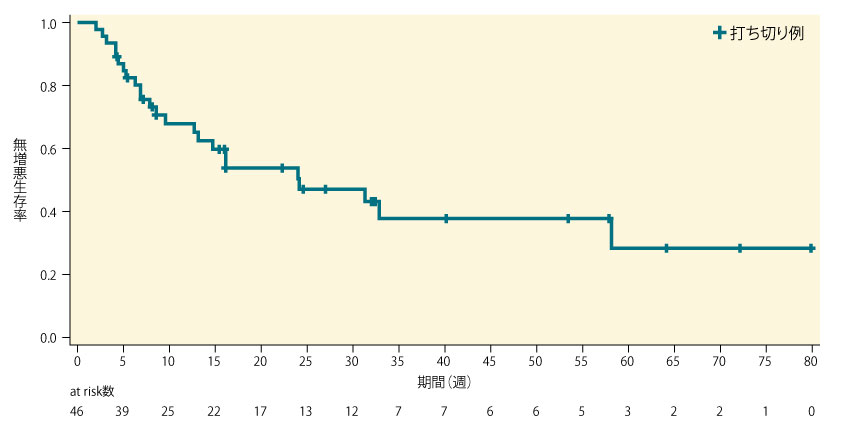
副次評価項目であるPFSは下図の通りで、データカットオフ時点で46例中24例(52.2%)にPDが確認され、22例(47.8%)が打ち切り*であった。PFSの中央値は、24.1週(95%CI:12.7, 58.1)[5.6ヵ月(95%CI:2.9, 13.4)]であった。
■PFS(IOERC評価、PPS)〔副次評価項目〕
-
(4)奏効期間(DOR)の中央値(IOERC評価、PPS)〔副次評価項目〕
副次評価項目であるDORは下図の通りで、データカットオフ時点で客観的奏効が認められた21例中5例(23.8%)にPDが確認され、16例(76.2%)が打ち切り*であった。DORの中央値は、50.1週(95%CI:23.3, -)[11.5ヵ月(95%CI:5.4, -)]であった。
■DOR(IOERC評価、PPS)〔副次評価項目〕
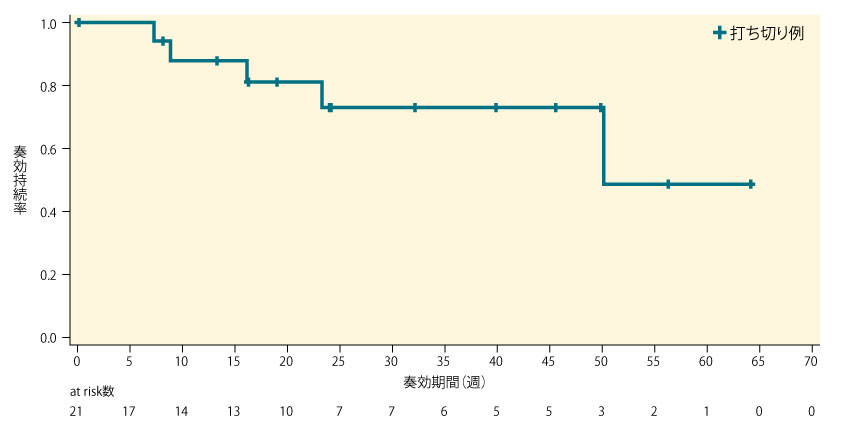
- *:許容できない毒性がみられたか、又は被験者が同意撤回した症例等
-
(5)全生存期間(OS)(PPS)〔探索的評価項目〕
探索的評価項目であるOSは下図の通りで、データカットオフ日までに、46例中14例(30.4%)の死亡が報告された。OSの中央値は、99.1週(95%CI:54.9, -)[22.8ヵ月(95%CI:12.6, -)]であった。
■OS(PPS)〔探索的評価項目〕
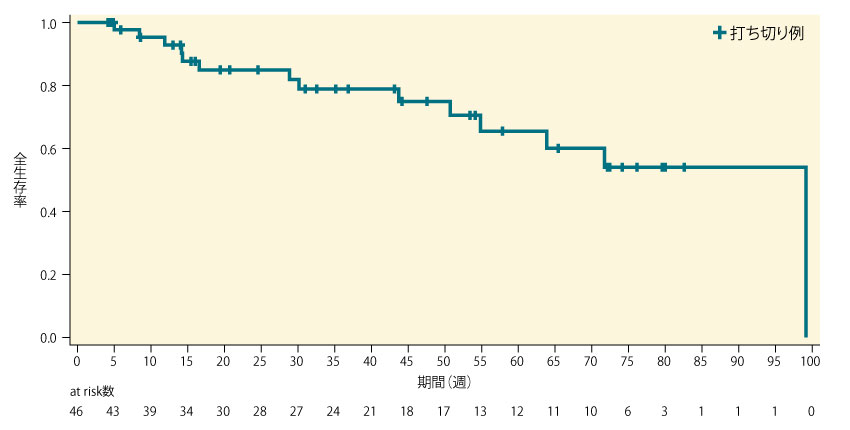
- *打ち切り例:許容できない毒性がみられたか、又は被験者が同意撤回した症例等
-
(6)病勢コントロール率(DCR)(IOERC評価、PPS)〔探索的評価項目〕
探索的評価項目であるDCRは、71.7%(95%CI:56.5, 84.0)であった。
■DCR及び最良総合効果(IOERC評価、PPS)〔探索的評価項目〕
例数
NCR
n(%)PR
n(%)SD
n(%)PD
n(%)〔探索的評価項目〕 DCR
n/N(%)95%CI PPS 46 5
(10.9)16
(34.8)12
(26.1)13
(28.3)33/46
(71.7)56.5, 84.0 - n/N:該当する被験者数/解析対象集団の被験者数
-
(7)奏効までの期間(TTR)(IOERC評価、PPS)〔探索的評価項目〕
探索的評価項目であるTTRの中央値は、奏効が認められた21例において8.1週(95%CI:8.0, 8.4)であった。
-
(8)腫瘍縮小効果(IRR・IOERC評価、PPS)〔探索的評価項目〕
ベースライン時に認められた腫瘍は、測定可能な節性及び節外性標的病変46例、皮膚病変8例に分類され、標的病変の総腫瘍サイズのベースラインからの最大変化、皮膚病変のmSWATスコア等を評価した腫瘍縮小効果は、下表の通りであった。
■腫瘍縮小効果(IRR・IOERC評価、PPS)〔探索的評価項目〕
例数
NCR
n(%)PR
n(%)SD
n(%)PD
n(%)NA
n(%)ORR
n/N(%)95%CI 測定可能な節性及び節外性標的病変
(IRR・IOERC評価)46 15
(32.6)8
(17.4)17
(37.0)5
(10.9)1
(2.2)23/46
(50.0)34.9, 65.1 皮膚病変
(IOERC評価*)8 2 2 3 1 0 4/8 - - *:治験担当医師のmSWATスコアを基にIOERCが評価
- NA:評価不能
- n/N:該当する被験者数/各病変が認められた被験者数
-
(9)部分集団別客観的奏効率(ORR)(PPS)〔探索的評価項目〕[サブグループ解析]
患者背景に基づく部分集団別のORR及び最良総合効果は下表の通りであった。
■部分集団別のORR及び最良総合効果(PPS)〔探索的評価項目〕
例数
NCR
n(%)PR
n(%)SD
n(%)PD
n(%)〔探索的評価項目〕 ORR
n/N(%)95%CI 再発又は難治性PTCL※ 再発 28 4
(14.3)11
(39.3)8
(28.6)5
(17.9)15/28
(53.6)33.9, 72.5 難治性 18 1
(5.6)5
(27.8)4
(22.2)8
(44.4)6/18
(33.3)13.3, 59.0 国別 日本 34 3
(8.8)15
(44.1)8
(23.5)8
(23.5)18/34
(52.9)35.1, 70.2 韓国 12 2
(16.7)1
(8.3)4
(33.3)5
(41.7)3/12
(25.0)5.5, 57.2 性別 男性 31 3
(9.7)12
(38.7)8
(25.8)8
(25.8)15/31
(48.4)30.2, 66.9 女性 15 2
(13.3)4
(26.7)4
(26.7)5
(33.3)6/15
(40.0)16.3, 67.7 年齢 <65歳 13 2
(15.4)5
(38.5)3
(23.1)3
(23.1)7/13
(53.8)25.1, 80.8 ≧65歳、<75歳 19 2
(10.5)8
(42.1)5
(26.3)4
(21.1)10/19
(52.6)28.9, 75.6 ≧75歳 14 1
(7.1)3
(21.4)4
(28.6)6
(42.9)4/14
(28.6)8.4, 58.1 前治療レジメン数 <3 29 5
(17.2)12
(41.4)7
(24.1)5
(17.2)17/29
(58.6)38.9, 76.5 ≧3 17 0
(0.0)4
(23.5)5
(29.4)8
(47.1)4/17
(23.5)6.8, 49.9 直近のがん治療からの期間 <3ヵ月 20 1
(5.0)6
(30.0)4
(20.0)9
(45.0)7/20
(35.0)15.4, 59.2 ≧3ヵ月 26 4
(15.4)10
(38.5)8
(30.8)4
(15.4)14/26
(53.8)33.4, 73.4 ベースライン時のECOG PS 0 24 2
(8.3)10
(41.7)6
(25.0)6
(25.0)12/24
(50.0)29.1, 70.9 1 21 3
(14.3)6
(28.6)6
(28.6)6
(28.6)9/21
(42.9)21.8, 66.0 2 1 0 0 0 1 0/1 - - ※: 各患者のハイヤスタ投与前の臨床情報から、直近の全身がん治療に対する反応に基づき、再発(直近の全身がん治療でCR、CRu又はPR)、難治性(直近の全身がん治療でSD又はPD)に分類した。
- n/N:該当する被験者数/部分集団別の被験者数
安全性(一次解析結果)
-
(10)安全性
■安全性の結果概要(SAF)
ハイヤスタ40mg(全体集団)
(n=55)全Gradeの有害事象 55(100.0) 治験薬と関連性のある全Gradeの有害事象 51(92.7) Grade 3以上の有害事象 46(83.6) Grade 3の有害事象 30(54.5) Grade 4の有害事象 15(27.3) Grade 5の有害事象 1(1.8) 治験薬と関連性のあるGrade 3以上の有害事象 42(76.4) 重篤な有害事象 14(25.5) 治験薬と関連性のある重篤な有害事象 10(18.2) 投与中止となった有害事象 18(32.7) 治験薬と関連性のある投与中止となった有害事象 17(30.9) 死亡に至った有害事象 1(1.8) - n(%)
■副作用及び有害事象の概要(SAF)
ハイヤスタ40mg(全体集団)
(n=55)主な副作用(10%以上) - ・血小板減少症※142例(76.4%)、好中球減少症※231例(56.4%)、白血球減少症※321例(38.2%)、リンパ球減少症※416例(29.1%)、貧血※5、食欲減退各12例(21.8%)、悪心11例(20.0%)、下痢10例(18.2%)、倦怠感8例(14.5%)、γ-GTP増加7例(12.7%)、血中ALP増加6例(10.9%)
Grade 3以上の有害事象 Grade 3
(2例以上)- ・血小板減少症※119例(34.5%)、好中球減少症※215例(27.3%)、白血球減少症※3、リンパ球減少症※4各10例(18.2%)、貧血※58例(14.5%)、発熱性好中球減少症、γ-GTP増加各3例(5.5%)、C-反応性蛋白増加、食欲減退、低ナトリウム血症、肺臓炎各2例(3.6%)
- ・治験薬と関連性のある有害事象は、血小板減少症※117例(30.9%)、好中球減少症※215例(27.3%)、リンパ球減少症※410例(18.2%)、白血球減少症※39例(16.4%)、貧血※55例(9.1%)、発熱性好中球減少症、γ-GTP増加各3例(5.5%)、C-反応性蛋白増加、食欲減退、低ナトリウム血症、肺臓炎各2例(3.6%)であった
Grade 4
(2例以上)- ・血小板減少症※19例(16.4%)、好中球減少症※25例(9.1%)、リンパ球減少症※4、低カリウム血症各2例(3.6%)
- ・治験薬と関連性のある有害事象は、血小板減少症※17例(12.7%)、好中球減少症※25例(9.1%)、リンパ球減少症※42例(3.6%)であった
重篤な有害事象 - ・発熱性好中球減少症2例(3.6%)、再生不良性貧血、不安定狭心症、疲労、発熱、ニューモシスチス・イロベチイ肺炎、咽頭炎、肺炎、C-反応性蛋白増加、低ナトリウム血症、PTCL-NOS、急性腎障害、上気道の炎症、肺臓炎、間質性肺疾患、末梢動脈閉塞性疾患各1例(1.8%)
- ・14例中10例で治験薬と関連性のある有害事象が認められた
投与中止となった有害事象 - ・好中球減少症※25例(9.1%)、血小板減少症※14例(7.3%)、リンパ球減少症※4、γ-GTP増加、肺臓炎各2例(3.6%)、白血球減少症※3、ニューモシスチス・イロベチイ肺炎、肺炎、脳性ナトリウム利尿ペプチド増加、血中ALP増加、PTCL-NOS、呼吸困難、間質性肺疾患各1例(1.8%)
- ・18例中17例で治験薬と関連性のある有害事象が認められた
死亡に至った有害事象 - ・肺炎1例(1.8%)
- ・死因は被験者の原疾患を考慮して治験薬との関連性はないと判断された
- ※1:血小板数減少を含む
- ※2:好中球数減少及び顆粒球減少症を含む
- ※3:白血球数減少を含む
- ※4:リンパ球数減少を含む
- ※5:ヘモグロビン減少を含む
■副作用種類別発現頻度(SAF)
ハイヤスタ40mg
(全体集団)
(n=55)1件以上の副作用が発現した症例 51(92.7) 血液及びリンパ系障害 47(85.5) 血小板減少症※1 42(76.4) 好中球減少症※2 31(56.4) 白血球減少症※3 21(38.2) リンパ球減少症※4 16(29.1) 貧血※5 12(21.8) 発熱性好中球減少症 3(5.5) 再生不良性貧血 1(1.8) 心臓障害 4(7.3) 動悸 2(3.6) 不整脈 1(1.8) 心嚢液貯留 1(1.8) 心房細動 1(1.8) 耳及び迷路障害 1(1.8) 回転性めまい 1(1.8) 眼障害 1(1.8) 結膜出血 1(1.8) 胃腸障害 25(45.5) 悪心 11(20.0) 下痢 10(18.2) 便秘 1(1.8) 嘔吐 1(1.8) 心窩部不快感 1(1.8) 消化不良 1(1.8) 胃炎 1(1.8) 腹痛 1(1.8) 腹部不快感 1(1.8) 齲歯 1(1.8) 一般・全身障害及び投与部位の状態 17(30.9) 倦怠感 8(14.5) 疲労 4(7.3) 末梢性浮腫 2(3.6) 発熱 2(3.6) 歩行障害 1(1.8) 無力症 1(1.8) 胸部不快感 1(1.8) 背部痛 1(1.8) 関節炎 1(1.8) 関節腫脹 1(1.8) 良性、悪性及び詳細不明の新生物(嚢胞及びポリープを含む) 1(1.8) PTCL-NOS 1(1.8) 神経系障害 4(7.3) 味覚異常 2(3.6) 頭痛 2(3.6) 浮動性めまい 1(1.8) 腎及び尿路障害 1(1.8) 蛋白尿 1(1.8) 呼吸器、胸郭及び縦隔障害 9(16.4) 肺臓炎 4(7.3) 呼吸困難 2(3.6) ハイヤスタ40mg
(全体集団)
(n=55)感染症及び寄生虫症 8(14.5) 気管支炎 2(3.6) サイトメガロウイルス感染 1(1.8) ニューモシスチス・イロベチイ肺炎 1(1.8) 上咽頭炎 1(1.8) 肺炎 1(1.8) 膀胱炎 1(1.8) 膿痂疹 1(1.8) 臨床検査 20(36.4) γ-GTP増加 7(12.7) 血中ALP増加 6(10.9) 心電図QT延長 5(9.1) AST増加 4(7.3) ALT増加 4(7.3) 体重減少 2(3.6) 好酸球数増加 2(3.6) 血中クレアチニン増加 2(3.6) C-反応性蛋白増加 2(3.6) リパーゼ増加 1(1.8) 心胸郭比増加 1(1.8) 心電図T波逆転 1(1.8) 脳性ナトリウム利尿ペプチド増加 1(1.8) 血中クレアチンホスホキナーゼ増加 1(1.8) 血中クレアチンホスホキナーゼMB増加 1(1.8) 血中免疫グロブリンA減少 1(1.8) 代謝及び栄養障害 16(29.1) 食欲減退 12(21.8) 低アルブミン血症 2(3.6) 低カリウム血症 2(3.6) 低カルシウム血症 2(3.6) 低ナトリウム血症 2(3.6) 糖尿病 1(1.8) 筋骨格系及び結合組織障害 7(12.7) 筋痙縮 3(5.5) 四肢痛 1(1.8) 筋肉疲労 1(1.8) 筋骨格硬直 1(1.8) 咳嗽 1(1.8) 胸水 1(1.8) 間質性肺疾患 1(1.8) 鼻出血 1(1.8) 皮膚及び皮下組織障害 12(21.8) 発疹 3(5.5) 蕁麻疹 3(5.5) 全身性そう痒症 2(3.6) 紫斑 2(3.6) ざ瘡様皮膚炎 1(1.8) 全身性剥脱性皮膚炎 1(1.8) 多形紅斑 1(1.8) 斑状丘疹状皮疹 1(1.8) 点状出血 1(1.8) - n(%)
- ※1:血小板数減少を含む
- ※2:好中球数減少及び顆粒球減少症を含む
- ※3:白血球数減少を含む
- ※4:リンパ球数減少を含む
- ※5:ヘモグロビン減少を含む
MedDRA ver.21.1、NCI-CTCAE ver.4.03
閲覧履歴
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。


 くすりに関する
くすりに関する