ハイヤスタ錠 臨床成績 再発又は難治性の成人T細胞白血病リンパ腫(ATL)
臨床成績 再発又は難治性の成人T細胞白血病リンパ腫(ATL)
日本人ATL患者を対象とする国内第Ⅱb相試験(HBI-8000-210試験)5)
社内資料:国内第Ⅱb相試験(HBI-8000-210試験)(承認時評価資料)
試験概要
- 目的:
- 再発又は難治性ATL※1を有する日本人患者を対象に、ハイヤスタを4週間のサイクルで週2回経口投与したときの有効性※2及び安全性を検討する。
- 対象:
-
モガムリズマブ投与歴があるもしくはモガムリズマブ不耐・適応外で1レジメン以上の全身化学療法を施行した、他の標準的治療法が適さない再発又は難治性ATLを有する日本人患者23例
有効性解析対象集団:最大の解析対象集団(FAS):23例
治験実施計画書に適合した対象集団(PPS):23例
SAF:23例
【主な組み入れ基準】- 組織学的又は細胞学的にATLと診断された患者
- 評価可能病変が1つ以上認められる患者
- ECOG PSが0~2である患者
- 余命が3ヵ月超と判断された患者
- 臓器移植を受けていない患者
- 同種幹細胞移植を受けていない患者
- 治験薬投与開始前12週間以内に自家幹細胞移植を受けていない患者
- 活動性感染症がない患者
- 心臓の異常又は不整脈を有さない患者
- 試験デザイン:
- 多施設共同・非盲検・非無作為化・単一群試験
- 方法:
- 対象患者にハイヤスタ40mgを食後(約30分後)に週2回(投与間隔3~4日)経口投与し、投与サイクルは1サイクルあたり4週間とした。
- 治療期間:
- PD又は最適な支持療法の実施にもかかわらず許容できない毒性が認められるまで。
- 評価項目:
-
- 主要評価項目
(検証的な解析結果): - ORR※3[ 独立総合効果判定委員会(IOERC)評価]
- 副次評価項目:
- ATL病型別ORR[サブグループ解析]、無増悪生存期間(PFS)の中央値(IOERC評価)、奏効期間(DOR)※4の中央値(IOERC評価)
- 探索的評価項目:
- 全生存期間(OS)、病勢コントロール率(DCR)※5、奏効までの期間(TTR)※6、腫瘍縮小効果[標的病変の総腫瘍サイズ、皮膚病変のSeverity-WeightedAssessment Tool改訂版(mSWAT)スコアのベースラインからの最大変化、異常リンパ球数のベースラインからの最大変化]、部分集団別ORR[サブグループ解析]、部分集団別PFS[サブグループ解析]、部分集団別OS[サブグループ解析]等
- 安全性評価項目:
- 有害事象等(MedDRA ver.21.1、NCI-CTCAE ver.4.03)
- 主要評価項目
- 解析計画:
- 安全性及び有効性のすべてのパラメータは、記述統計を用いて解析した。カテゴリー変数は度数分布(被験者数及び割合)を用いて要約した。連続変数は平均値、標準偏差、中央値、最小値及び最大値を用いて要約した。Time-to-event型変数はKaplan-Meier法及びKaplan-Meier曲線の図示による中央値の推定を用いて要約した。主要評価項目である有効性の解析は、IOERC及び独立画像判定(IRR)による評価に基づきPPSを対象とし、ORRは正確な二項分布の95%CIで要約した。
サブグループ解析として、性別、年齢、ECOG PS、ATL病型、ATLサブセット、前治療レジメン数、直近のがん治療、過去のモガムリズマブ治療、直近のがん治療からの期間の評価が事前規定された。CIの下限値が5%の閾値より高い場合、ORRは5%より有意に優れていると結論付けるものとした。本治験の目標ORRを30%とした。なお、カットオフ日(最終被験者の治療終了時評価完了時点)までのデータを基に解析した。
- ※1:急性型、リンパ腫型又は予後不良因子(血中尿素窒素高値、乳酸脱水素酵素高値又は血清アルブミン低値のいずれか)を有する慢性型のATL
- ※2:治療効果及びATLのPDは、修正した国際コンセンサス会議の基準(Tsukasaki 2009)及びmSWAT(Stevens 2002、Olsen 2011)に準じて評価した
- ※3:CR、CRu又はPRが認められた患者の割合
- ※4:最初にCR、CRu又はPRが認められてからPD又は死亡までの期間。打ち切りの場合は最後の総合効果判定日
- ※5:CR、CRu、PR又はSDが認められた患者の割合
- ※6:初回投与からPR以上の効果が認められるまでの期間
有効性
-
(1)客観的奏効率(ORR)(IOERC評価、PPS)〔主要評価項目、検証的な解析結果〕
IOERC評価によるORR及び最良総合効果は下表の通りであった。
主要評価項目であるPPSのORRは30.4%(7/23例、95%CI:13.2, 52.9)であり、本試験の目標である30%を超え、95%CIの下限が本試験で規定した5%の閾値を上回っていた。■ORR及び最良総合効果(IOERC評価、PPS)〔主要評価項目〕
例数
NCR
n(%)CRu
n(%)PR
n(%)SD
n(%)PD
n(%)〔主要評価項目〕 ORR
n/N(%)95%CI PPS 23 1
(4.3)0
(0.0)6
(26.1)5
(21.7)11
(47.8)7/23
(30.4)13.2, 52.9 - n/N:該当する被験者数/解析対象集団の被験者数
-
(2)ATL病型別客観的奏効率(ORR)(IOERC評価、PPS)〔副次評価項目〕[サブグループ解析]
ベースライン時のATL病型は、急性型が13例、リンパ腫型が8例、予後不良因子を有する慢性型が2例であり、副次評価項目であるATL病型別ORR及び最良総合効果は下表の通りであった。
■ATL病型別ORR及び最良総合効果(IOERC評価、PPS)〔副次評価項目〕
例数
NCR
n(%)CRu
n(%)PR
n(%)SD
n(%)PD
n(%)〔副次評価項目〕 ORR
n/N(%)95%CI 急性型 13 1
(7.7)0
(0.0)5
(38.5)2
(15.4)5
(38.5)6/13
(46.2)19.2, 74.9 リンパ腫型 8 0 0 1 2 5 1/8 - 予後不良因子を有する慢性型 2 0 0 0 1 1 0/2 - - n/N:該当する被験者数/ATL病型別の被験者数
-
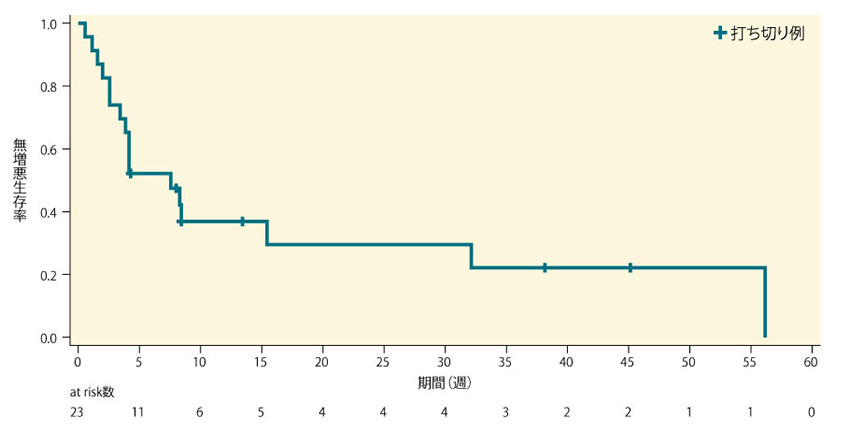
(3)無増悪生存期間(PFS)の中央値(IOERC評価、PPS)〔副次評価項目〕
副次評価項目であるPFSは下図の通りで、データカットオフ時点で23例中17例(73.9%)にPDが確認され、6例が打ち切り*であった。PFSの中央値は、7.6週(95%CI:3.4, 32.1)[1.7ヵ月(95%CI:0.8, 7.4)]であった。
■PFS(IOERC評価、PPS)〔副次評価項目〕
-
(4)奏効期間(DOR)の中央値(IOERC評価、PPS)〔副次評価項目〕
副次評価項目であるDORについて、データカットオフ時点で客観的奏効が認められた7例中3例にPDが確認され、4例が打ち切り*であった。DORの中央値は、28.1週(6.5ヵ月)であった。
- *:許容できない毒性がみられたか、又は被験者が同意撤回した症例等
-
(5)全生存期間(OS)(PPS)〔探索的評価項目〕
探索的評価項目であるOSの中央値は、52.7週(95%CI:9.3, -)[12.1ヵ月(95%CI:2.1, -)]であった。
データカットオフ日までに、23例中12例(52.2%)の死亡が報告された。 -
(6)病勢コントロール率(DCR)(IOERC評価、PPS)〔探索的評価項目〕
探索的評価項目であるDCRは、52.2%(95%CI:30.6, 73.2)であった。
■DCR及び最良総合効果(IOERC評価、PPS)〔探索的評価項目〕
例数
NCR
n(%)CRu
n(%)PR
n(%)SD
n(%)PD
n(%)〔探索的評価項目〕 DCR
n/N(%)95%CI PPS 23 1
(4.3)0
(0.0)6
(26.1)5
(21.7)11
(47.8)12/23
(52.2)30.6, 73.2 - n/N:該当する被験者数/解析対象集団の被験者数
-
(7)奏効までの期間(TTR)(IOERC評価、PPS)〔探索的評価項目〕
探索的評価項目であるTTRの中央値は、客観的奏効が認められた7例において13.4週であった。
-
(8)腫瘍縮小効果(IRR・IOERC評価、PPS)〔探索的評価項目〕
ベースライン時に認められた腫瘍は、測定可能な節性及び節外性標的病変20例、皮膚病変8例、末梢血病変5例に分類され、標的病変の総腫瘍サイズ、皮膚病変のmSWATスコア及び末梢血データ(異常リンパ球数)のベースラインからの最大変化等を評価した腫瘍縮小効果は、下表の通りであった。
■腫瘍縮小効果(IRR・IOERC評価、PPS)〔探索的評価項目〕
例数
NCR
n(%)CRu
n(%)PR
n(%)SD
n(%)PD
n(%)NA
n(%)ORR
n/N(%)95%CI 測定可能な節性及び節外性標的病変
(IRR・IOERC評価)20 4
(20.0)0
(0.0)2
(10.0)7
(35.0)4
(20.0)3
(15.0)6/20
(30.0)11.9, 54.3 皮膚病変
(IOERC評価*1)8 2 - 3 1 2 0 5/8 - 末梢血病変
(IOERC評価*2)5 1 - 2 1 1 0 3/5 - - *1:治験担当医師のmSWATスコアを基にIOERCが評価
- *2:実施施設の検査結果を基にIOERCが評価
- NA:該当しない
- n/N:該当する被験者数/各病変が認められた被験者数
-
(9)部分集団別客観的奏効率(ORR)(PPS)〔探索的評価項目〕[サブグループ解析]
患者背景に基づく部分集団別のORR及び最良総合効果は下表の通りであった。
■部分集団別のORR及び最良総合効果(PPS)〔探索的評価項目〕
例数
NCR
n(%)CRu
n(%)PR
n(%)SD
n(%)PD
n(%)〔探索的評価項目〕 ORR
n/N(%)95%CI 再発、再燃又は難治性ATL※ 再発又は再燃 18 1
(5.6)0
(0.0)6
(33.3)3
(16.7)8
(44.4)7/18
(38.9)17.3, 64.3 再発 5 1 0 3 1 0 4/5 - 再燃 13 0
(0.0)0
(0.0)3
(23.1)2
(15.4)8
(61.5)3/13
(23.1)5.0, 53.8 難治性 5 0 0 0 2 3 0/5 - 性別 男性 15 0
(0.0)0
(0.0)2
(13.3)4
(26.7)9
(60.0)2/15
(13.3)1.7, 40.5 女性 8 1 0 4 1 2 5/8 - 年齢 <65歳 1 0 0 1 0 0 1/1 - ≧65歳、<75歳 13 1
(7.7)0
(0.0)4
(30.8)2
(15.4)6
(46.2)5/13
(38.5)13.9, 68.4 ≧75歳 9 0 0 1 3 5 1/9 - 前治療レジメン数 <3 11 1
(9.1)0
(0.0)4
(36.4)1
(9.1)5
(45.5)5/11
(45.5)16.7, 76.6 ≧3 12 0
(0.0)0
(0.0)2
(16.7)4
(33.3)6
(50.0)2/12
(16.7)2.1, 48.4 直近のがん治療 化学療法のみ 6 0 0 1 2 3 1/6 - モガムリズマブ併用 8 1 0 3 1 3 4/8 - モガムリズマブ単独 6 0 0 2 0 4 2/6 - レナリドミド単独 3 0 0 0 2 1 0/3 - 過去のモガムリズマブ単独療法 あり 12 0
(0.0)0
(0.0)2
(16.7)3
(25.0)7
(58.3)2/12
(16.7)2.1, 48.4 なし 11 1
(9.1)0
(0.0)4
(36.4)2
(18.2)4
(36.4)5/11
(45.5)16.7, 76.6 過去のモガムリズマブ併用療法 あり 11 1
(9.1)0
(0.0)4
(36.4)2
(18.2)4
(36.4)5/11
(45.5)16.7, 76.6 なし 12 0
(0.0)0
(0.0)2
(16.7)3
(25.0)7
(58.3)2/12
(16.7)2.1, 48.4 直近のがん治療からの期間 <3ヵ月 12 0
(0.0)0
(0.0)0
(0.0)4
(33.3)8
(66.7)0/12
(0.0)0.0, 26.5 ≧3ヵ月 11 1
(9.1)0
(0.0)6
(54.5)1
(9.1)3
(27.3)7/11
(63.6)30.8, 89.1 ベースライン時のECOG PS 0 12 1
(8.3)0
(0.0)5
(41.7)3
(25.0)3
(25.0)6/12
(50.0)21.1, 78.9 1 10 0
(0.0)0
(0.0)1
(10.0)2
(20.0)7
(70.0)1/10
(10.0)0.3, 44.5 2 1 0 0 0 0 1 0/1 - - ※: 各患者のハイヤスタ投与前の臨床情報から、直近の全身がん治療に対する反応に基づき、再発(直近の全身がん治療でCR又はCRu)、再燃(直近の全身がん治療でPR又はSD)、難治性(直近の全身がん治療でPD)に分類した。
- n/N:該当する被験者数/部分集団別の被験者数
安全性
-
(10)安全性
■安全性の結果概要(SAF)
ハイヤスタ40mg
(n=23)全Gradeの有害事象 23(100.0) 治験薬と関連性のある全Gradeの有害事象 23(100.0) Grade 3以上の有害事象 18(78.3) Grade 3の有害事象 9(39.1) Grade 4の有害事象 9(39.1) 治験薬と関連性のあるGrade 3以上の有害事象 18(78.3) 重篤な有害事象 7(30.4) 治験薬と関連性のある重篤な有害事象 6(26.1) 投与中止となった有害事象 9(39.1) 治験薬と関連性のある投与中止となった有害事象 9(39.1) 死亡に至った有害事象 0(0.0) - n(%)
■副作用及び有害事象の概要(SAF)
ハイヤスタ40mg
(n=23)主な副作用(10%以上) - ・血小板減少症※118例(78.3%)、好中球減少症※212例(52.2%)、白血球減少症※310例(43.5%)、貧血※49例(39.1%)、食欲減退8例(34.8%)、倦怠感7例(30.4%)、下痢5例(21.7%)、体重減少、味覚異常各4例(17.4%)、悪心、低アルブミン血症各3例(13.0%)
Grade 3以上の有害事象 Grade 3
(2例以上)- ・血小板減少症※16例(26.1%)、好中球減少症※2、白血球減少症※3各7例(30.4%)、貧血※45例(21.7%)、疲労2例(8.7%)
- ・いずれの有害事象も治験薬と関連性があると判定された
Grade 4
(2例以上)- ・血小板減少症※16例(26.1%)、好中球減少症※23例(13.0%)
- ・いずれの有害事象も治験薬と関連性があると判定された
重篤な有害事象 - ・血小板減少症※12例(8.7%)、好中球減少症※2、動悸、ニューモシスチス・イロベチイ肺炎、尿路感染、急性呼吸不全、間質性肺疾患各1例(4.3%)
- ・急性呼吸不全を除くいずれの有害事象も治験薬と関連性があると判定された
投与中止となった有害事象 - ・血小板減少症※14例(17.4%)、好中球減少症※23例(13.0%)、疲労、ニューモシスチス・イロベチイ肺炎、血中ALP増加、γ-グルタミルトランスペプチダーゼ(GTP)増加、間質性肺疾患各1例(4.3%)
- ・9例全例で治験薬と関連性のある有害事象が認められた
死亡に至った有害事象 - ・なし
- ※1:血小板数減少を含む
- ※2:好中球数減少及び顆粒球減少症を含む
- ※3:白血球数減少を含む
- ※4:ヘモグロビン減少を含む
■副作用種類別発現頻度(SAF)
ハイヤスタ40mg
(n=23)1件以上の副作用が発現した症例 23(100.0) 血液及びリンパ系障害 19(82.6) 血小板減少症※1 18(78.3) 好中球減少症※2 12(52.2) 白血球減少症※3 10(43.5) 貧血※4 9(39.1) リンパ球減少症※5 2(8.7) 好酸球増加症 1(4.3) 発熱性好中球減少症 1(4.3) 心臓障害 2(8.7) 第一度房室ブロック 1(4.3) 動悸 1(4.3) 胃腸障害 7(30.4) 下痢 5(21.7) 悪心 3(13.0) 腹痛 1(4.3) 口内炎 1(4.3) 一般・全身障害及び投与部位の状態 10(43.5) 倦怠感 7(30.4) 疲労 2(8.7) 発熱 2(8.7) 悪寒 1(4.3) 末梢性浮腫 1(4.3) 感染症及び寄生虫症 5(21.7) サイトメガロウイルス感染 1(4.3) 医療機器関連感染 1(4.3) 口腔カンジダ症 1(4.3) ニューモシスチス・イロベチイ肺炎 1(4.3) 皮膚感染 1(4.3) 尿路感染 1(4.3) 臨床検査 8(34.8) 体重減少 4(17.4) AST増加 2(8.7) ハイヤスタ40mg
(n=23)γ-GTP増加 2(8.7) ALT増加 1(4.3) 血中ALP増加 1(4.3) 好酸球数増加 1(4.3) リパーゼ増加 1(4.3) 代謝及び栄養障害 12(52.2) 食欲減退 8(34.8) 低アルブミン血症 3(13.0) 低ナトリウム血症 2(8.7) 低カリウム血症 1(4.3) 低リン酸血症 1(4.3) 筋骨格系及び結合組織障害 1(4.3) 関節痛 1(4.3) 神経系障害 7(30.4) 味覚異常 4(17.4) 味覚消失 1(4.3) 頭痛 1(4.3) 傾眠 1(4.3) 腎及び尿路障害 1(4.3) 尿瘻 1(4.3) 呼吸器、胸郭及び縦隔障害 2(8.7) 鼻出血 1(4.3) 間質性肺疾患 1(4.3) 皮膚及び皮下組織障害 5(21.7) 紅斑 1(4.3) 多形紅斑 1(4.3) 光線過敏性反応 1(4.3) そう痒症 1(4.3) 発疹 1(4.3) 皮膚潰瘍 1(4.3) 血管障害 1(4.3) 高血圧 1(4.3) - n(%)
- ※1:血小板数減少を含む
- ※2:好中球数減少及び顆粒球減少症を含む
- ※3:白血球数減少を含む
- ※4:ヘモグロビン減少を含む
- ※5:リンパ球数減少を含む
MedDRA ver.21.1、NCI-CTCAE ver.4.03
閲覧履歴
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。


 くすりに関する
くすりに関する