製品Q&A
コスタイベ筋注用
コスタイベ筋注用の副反応について教えてください。
2024年10月更新
#安全性
コスタイベ筋注用の副反応については次の情報があります。
1)電子添文には次の記載があります。
11. 副反応
次の副反応があらわれることがあるので、観察を十分に行い、異常が認められた場合には適切な処置を行うこと。
11.1 重大な副反応
11.1.1 ショック、アナフィラキシー(頻度不明)
[2.3 参照],[8.4 参照],[9.1.6 参照]
11.1.2 心筋炎、心膜炎(頻度不明)
[8.6 参照],[15.1.1 参照],[15.1.2 参照]
11.2 その他の副反応
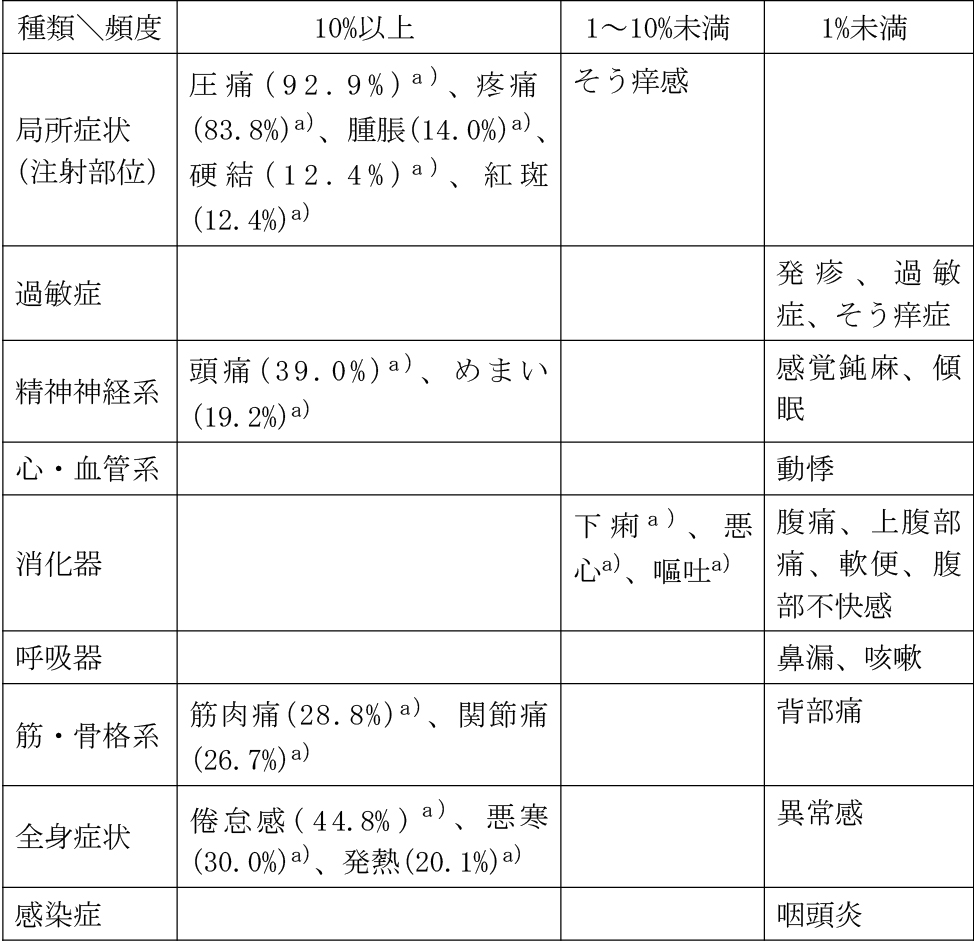
a)臨床試験において日誌により収集した副反応の発現割合
注)海外臨床試験(ARCT-154-01試験第Ⅲbパート)及び国内臨床試験(ARCT-154-J01試験及びARCT-2301-J01試験)で収集した事象の発現割合をそれぞれ算出し、共通して発現の認められた事象についてはより高い発現割合の値を記載した。
※[参照]については、最新の電子添文をご確認ください。
2)審議結果報告書には次の記載があります。
7.R.3.2 注目すべき有害事象について
(2)心筋炎・心膜炎、ギラン・バレー症候群、VAED・VAERD
提出されたいずれの試験においても、心筋炎・心膜炎、ギラン・バレー症候群及びVAED・VAERDに関連する有害事象の発現は認められなかった。
(中略)
既承認RNAワクチンで注目すべき有害事象とされている心筋炎・心膜炎、ギラン・バレー症候群及びVAED・VAERDについて、①これらの有害事象は発現頻度が低く、臨床試験成績のみから明確なリスク評価を行うことは困難と考えること、及び②本剤が既承認RNAワクチンと同様のRNAワクチンであることを踏まえると、製造販売後にこれらの事象が発現する可能性は否定できないことから、いずれも注意が必要であり、申請者の説明どおり、注意喚起等を行うことは適当と判断した。
参考資料:
1)コスタイベ筋注用 電子添文
2)コスタイベ筋注用 審議結果報告書(2023年11月28日)
管理番号:KO-14
製品に関してご不明点がございましたら弊社MRまたはくすり相談室にお問合せください。
ご利用にあたっての注意
製品Q&Aは製品の適正使用に関する参考情報であり、すべての事例にあてはまるものではございません。
国内で承認された効能・効果、用法・用量の範囲外の情報を含む場合がありますが、そのような使用方法を当社として推奨するものではありません。
製品Q&Aの利用に伴って生じた結果につきましては責任を負いかねますのでご了承ください。保険審査に関しては、弊社としてはお答えしかねます。各地域の審査機関(国保連合会・支払基金など)にご確認ください。
本内容を無断で複製すること、改変すること、第三者に公開すること等を禁止します。製品Q&Aは、予告なく更新・修正・削除される可能性があります。必ずしも最新の情報とは限りませんので、 製品のご使用にあたっては最新の電子化された添付文書等をご確認ください。
製品に関してご不明点がございましたら弊社MRまたはくすり相談室にお問合せください。
関連リンク
閲覧履歴


 くすりに関する
くすりに関する