ビラノア錠・OD錠 蕁麻疹・皮膚疾患に伴うそう痒に対する効果
※ 承認された効能又は効果は次の通りです。
〇アレルギー性鼻炎
〇蕁麻疹
〇皮膚疾患(湿疹・皮膚炎、皮膚そう痒症)に伴うそう痒
慢性蕁麻疹患者を対象とした臨床第Ⅱ/Ⅲ相試験 7)、8)(承認時評価資料)
本試験は、用量反応性の検討を目的の1つとして実施されました。
そのため、紹介する結果には一部承認用量と異なる成績が含まれています。

![TSSの期間平均変化量[ベースライン(投与の4~1日前の計4日間の平均スコア)に対する投与8~14日目の計7日間の平均スコアの変化量] 副次評価項目 TSSの変化量の経日推移 副次評価項目](/img/product/bl/pruritus_001_02.png)
安全性
副作用(臨床検査値の異常変動を含む)はビラノア20mg群で101例中2例(2.0%)、ビラノア10mg群で100例中6例(6.0%)、プラセボ群で103例中3例(2.9%)に認められた。発現した副作用は、ビラノア20mg群で血中ビリルビン増加、頭痛各1例(1.0%)、ビラノア10mg群で傾眠2例(2.0%)、腹部不快感、便秘、悪心、倦怠感、口渇各1例(1.0%)、プラセボ群で口内炎、歯痛、胸痛、口渇、傾眠各1例(1.0%)であった。本試験において重篤な副作用及び投与中止にいたる副作用の発現、死亡例は認められなかった。
7) 慢性蕁麻疹患者を対象としたTAC-202の臨床第Ⅱ/Ⅲ相試験, 社内資料, 研究報告書No.643(2016)<承認時評価資料>
8) Hide M, et al.: Allergol Int., 66, 317(2017)
本研究は大鵬薬品工業株式会社の資金により行われた。
本論文の著者には大鵬薬品工業株式会社の社員と大鵬薬品工業株式会社から報酬を受領している者が含まれる。
※承認された用法及び用量は次の通りです。
通常、成人にはビラスチンとして1回20mgを1日1回空腹時に経口投与する。
慢性蕁麻疹及び皮膚疾患(湿疹・皮膚炎、痒疹※、皮膚そう痒症)に伴うそう痒患者を対象とした臨床第Ⅲ相長期投与試験 9)、10)(承認時評価資料)

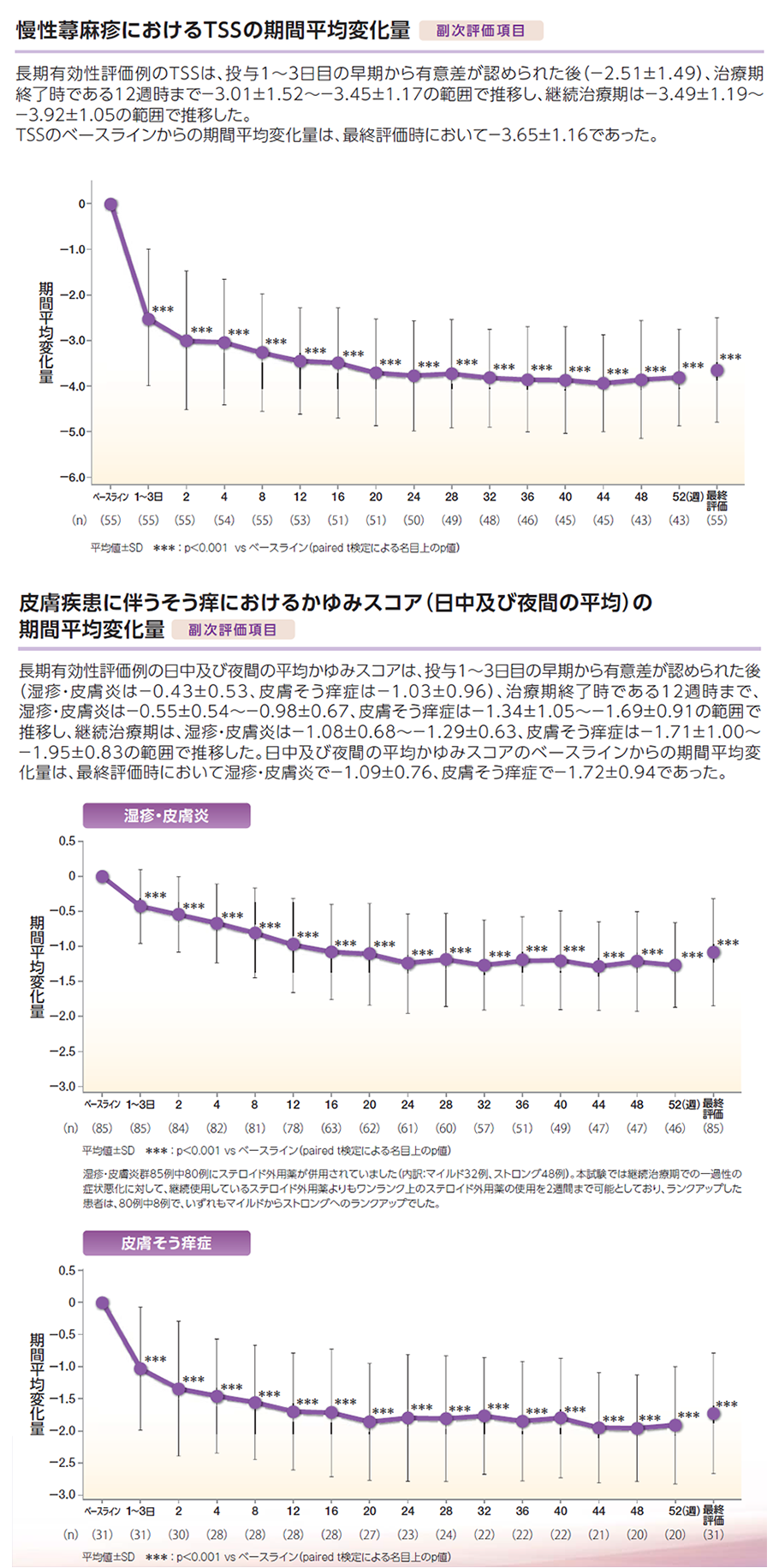
安全性 主要評価項目
副作用(臨床検査値の異常変動を含む)は197例中5例(2.5%)に認められた。発現した副作用は、傾眠2例(1.0%)、アスパラギン酸アミノトランスフェラーゼ増加、γ-グルタミルトランスフェラーゼ増加、夜間頻尿各1例(0.5%)であった。
本試験において重篤な副作用及び投与中止にいたる副作用の発現、死亡例は認められなかった。
52週間の長期投与で発現率が高くなる副作用や遅発性の副作用は認められなかった。
9) 慢性蕁麻疹及び皮膚疾患に伴うそう痒患者を対象としたTAC-202の臨床第Ⅲ相長期投与試験,社内資料,研究報告書No.644(2016)<承認時評価資料>
10) Yagami A, et al.: J Dermatol., 44, 375(2017)
本研究は大鵬薬品工業株式会社の資金により行われた。
本論文の著者には大鵬薬品工業株式会社の社員と大鵬薬品工業株式会社から報酬を受領している者が含まれる。
※ 承認された効能又は効果は次の通りです。
〇アレルギー性鼻炎
〇蕁麻疹
〇皮膚疾患(湿疹・皮膚炎、皮膚そう痒症)に伴うそう痒
閲覧履歴
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。


 くすりに関する
くすりに関する