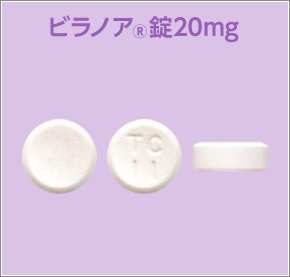
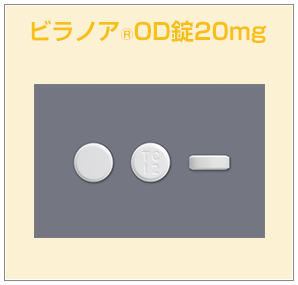
ビラノア錠・OD錠 概要・製品特性
- ■禁忌
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
- ■効能又は効果
〇アレルギー性鼻炎
〇蕁麻疹
〇皮膚疾患(湿疹・皮膚炎、皮膚そう痒症)に伴うそう痒 - ■用法及び用量
通常、成人にはビラスチンとして1回20mgを1日1回空腹時に経口投与
する。
- 1. 1日1回※1投与で、アレルギー性鼻炎、蕁麻疹、皮膚疾患に伴うそう痒※2に対して、効果を発現し、その効果は持続します。
-
- ●スギ花粉曝露で誘発した鼻症状はプラセボと比較して投与45分後から有意差が認められ、その効果は24時間持続しました。1)、2)
- ●通年性アレルギー性鼻炎の鼻症状はプラセボと比較して投与1日目より有意差が認められました。3)、4)
季節性及び通年性アレルギー性鼻炎の鼻症状は投与1~3日目からベースラインと比較して有意差が認められ、その効果は減弱することなく季節性は4週まで、通年性は52週まで持続が確認されました。5)、6) - ●慢性蕁麻疹症状は投与1日目からプラセボと比較して有意差が認められました。7)、8)
慢性蕁麻疹及び皮膚疾患に伴うそう痒※2のいずれの症状も投与1~3日目からベースラインと比較して有意差が認められ、その効果は減弱することなく52週まで持続が確認されました。9)、10)
- 2. 薬物代謝をほとんど受けずに未変化体のまま尿中(28.3%)及び糞中(66.5%)に排泄されます。11)
また、薬物代謝酵素(CYP)の阻害及び誘導作用を示しませんでした。(in vitro)12)、13) - 3. ビラノアOD錠20mgは水なしでも服用可能な口腔内崩壊錠です。
- ●ビラノアOD錠20mgはビラノア錠20mgとの生物学的同等性が確認されています。14)
- 4. 重大な副作用として、ショック、アナフィラキシーがあらわれることがあります。
国内臨床試験において、675例#中16例(2.4%)に副作用が報告されました。
主な副作用は、眠気4例(0.6%)、口渇及び頭痛が各2例(0.3%)でした(承認時)。
なお、添付文書の副作用及び臨床成績の安全性の結果をご参照ください。
#:痒疹※224例を含む
1) スギ花粉曝露室を用いたTAC-202の前期臨床第Ⅱ相試験,社内資料, 研究報告書No.640(2016)<承認時評価資料>
2) Hashiguchi K, et al.: Allergol Int.,66,123(2017)
本研究は大鵬薬品工業株式会社の資金により行われた。
本論文の著者には大鵬薬品工業株式会社の社員と大鵬薬品工業株式会社から報酬を受領している者が含まれる。
3) 通年性アレルギー性鼻炎患者を対象としたTAC-202の臨床第Ⅲ相試験,社内資料, 研究報告書No.641(2016)<承認時評価資料>
4) Okubo K,et al.: Allergol Int.,66,97(2017)
本研究は大鵬薬品工業株式会社の資金により行われた。
本論文の著者には大鵬薬品工業株式会社の社員と大鵬薬品工業株式会社から報酬を受領している者が含まれる。
5) 通年性及び季節性アレルギー性鼻炎患者を対象としたTAC-202の臨床第Ⅲ相長期投与試験,社内資料, 研究報告書No.642(2016)<承認時評価資料>
6) Okubo K, et al.: Auris Nasus Larynx, 44, 294(2017)
本研究は大鵬薬品工業株式会社の資金により行われた。
本論文の著者には大鵬薬品工業株式会社の社員と大鵬薬品工業株式会社から報酬を受領している者が含まれる。
7) 慢性蕁麻疹患者を対象としたTAC-202の臨床第Ⅱ/Ⅲ相試験,社内資料, 研究報告書No.643(2016)<承認時評価資料>
8) Hide M, et al.: Allergol Int., 66, 317(2017)
本研究は大鵬薬品工業株式会社の資金により行われた。
本論文の著者には大鵬薬品工業株式会社の社員と大鵬薬品工業株式会社から報酬を受領している者が含まれる。
9) 慢性蕁麻疹及び皮膚疾患に伴うそう痒患者を対象としたTAC-202の臨床第Ⅲ相長期投与試験,社内資料, 研究報告書No.644(2016)<承認時評価資料>
10) Yagami A, et al.: J Dermatol., 44, 375(2017)
本研究は大鵬薬品工業株式会社の資金により行われた。
本論文の著者には大鵬薬品工業株式会社の社員と大鵬薬品工業株式会社から報酬を受領している者が含まれる。
11) Mair SJ: A phase I study to investigate the absorption, metabolism and excretion of [14C]-bilastine following oral administration to healthy volunteers,社内資料, 研究報告書No.595(2016)
12) Johanning K: In Vitro Assessment of Human Liver Cytochrome P450 Inhibition Potential of Bilastine,社内資料,研究報告書No.586(2016)
13) Johanning K: in vitro Assessment of Cytochrome P450 Induction Potential of Bilastine in Primary Human Hepatocytes,社内資料, 研究報告書No.587(2016)
14) 健康成人を対象としたTAC-202 錠とTAC-202OD 錠の生物学的同等性試験,社内資料, 研究報告書No.RR21CD001(2021)<承認時評価資料>
※1 承認された用法及び用量は次の通りです。
通常、成人にはビラスチンとして1回20mgを1日1回空腹時に経口投与する。
※2 承認された効能又は効果は次の通りです。
〇アレルギー性鼻炎
〇蕁麻疹
〇皮膚疾患(湿疹・皮膚炎、皮膚そう痒症)に伴うそう痒
閲覧履歴
Meiji Seikaファルマ株式会社
医療関係者向けサイト
このサイトは、国内の医療関係者(医師・薬剤師・看護師等)を対象に、弊社の医療用医薬品等に関する情報提供を目的として作成されています。
一般・患者の方への情報提供を目的としたものではありませんのでご了承ください。
当サイトは医療関係者の方への
情報提供を目的としています。


 くすりに関する
くすりに関する